
Брой 6/2021
Пациент на 62 години с 12-годишна анамнеза на диабет тип 2 (T2D) се явява в лекарски кабинет за проследяваща визита. Предишната му медицинска анамнеза е сигнификантна за инфаркт на миокарда (MI) на 55-годишна възраст и хипертония, лекувана в момента с ангиотензин-рецепторен блокер (ARB).
Той съобщава, че се чувства доста добре и се шегува, че и изпитва само обикновени болежки, типични за „старо“ момче като него. Лекарят открива, че нощното му виждане се влошава и че и се появяват оплаквания от замъглено зрение на двете очи. Медицинската анамнеза на пациента и резултатите от направения му физикален преглед са показани в Taбл. 1.
Taбл. 1. Настояща анамнеза и резултати от прегледа
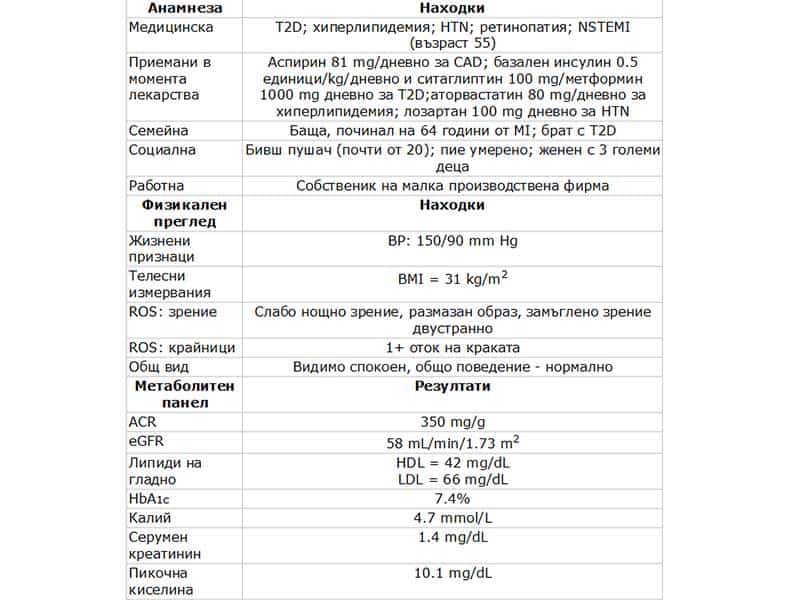
ACR = съотношение албумин-креатинин; BMI = индекс на телесна маса; BP = кръвно налягане; CAD = коронарна артериална болест; eGFR = оценена скорост на гломерулна филтрация; HbA1c = гликиран хемоглобин; HDL = липопротеин с висока плътност; HTN = хипертония; LDL = липопротеин с ниска плътност; NSTEMI = миокарден инфаркт без ST-елевация; OU = oculus uterque (двете очи).
Въпрос
Какъв е риска при пациента от прогресия на хронична бъбречна недостатъчност (CKD)?
- Нисък
- Умерен
- Висок
- Много висок
Верен отговор: Много висок
CKD се класифицира въз основа нивото на функциониране на бъбрека, измерено чрез оценена GFR (eGFR) и албуминоурия. Пациент с eGFR <60 mL/min/1.73 m2 и отделяне на албумин >300 mg/g има CKD и е изложен на много висок риск от прогресия до краен стадий на бъбречно заболяване (ESRD), повишена заболеваемост и сърдечносъдова (CV) смъртност. CV смъртността се е повишила 2 пъти при пациенти с остър коронарен синдром (ACS), които имат също CKD, в сравнение с пациенти с ACS и нормална бъбречна функция.
CKD се категоризира в 5 нива на eGFR и 3 степени на албуминоурия.(Taбл. 2.) Ниската eGFR и повишена албуминоурия се свързват с по-висок кардиоренален риск. Смъртността от CV при пациенти със степен 3 CKD е приблизително двойно по-висока, отколкото при пациенти с нормална бъбречна функция.
Taбл 2. Система на степенуване на CKD
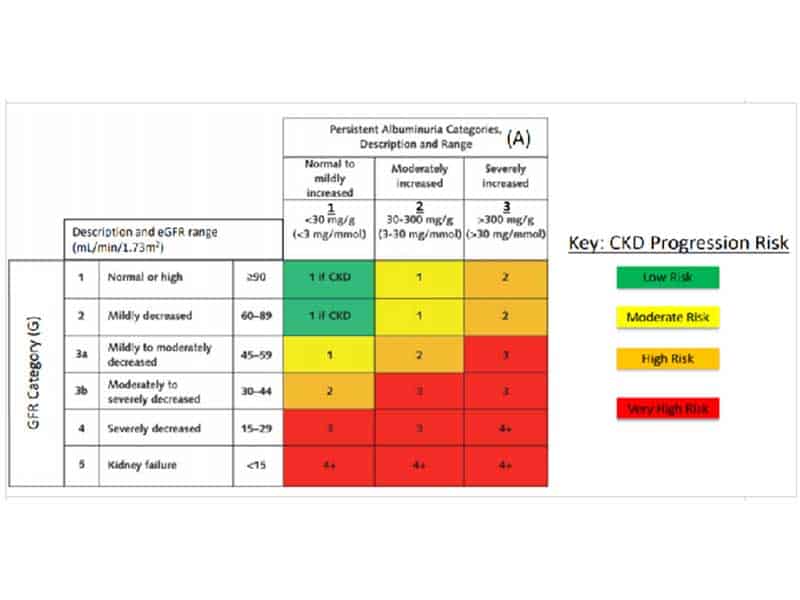
Числата във всяко квадратче представляват препоръки за честотата на мониториране/година.
Лекарят обяснява на пациента, че лабораторните му резултати показват, че има бъбречно нарушение, което повишава риска от друга сърдечна атака. Пациентът отговаря, че това звучи сериозно, но че се чувства добре. Лекарят отвръща, че знае че е така и че това не е необичайно, а също така че не е необичайно за човек с анамнеза за T2D и хипертония от дълги години да развива бъбречно заболяване. Но го окуражава, че за щастие има доста неща, които могат да се направят.
Факторите, свързани с прогресията на CKD и повишения риск от CV се припокриват широко. При пациенти с CKD и диабет, стратегиите на лечение трябва да бъдат мултифакторни, относно хиперурикемията, заедно с изменяемите CV рискови фактори като хипергликемия, хипертония и хиперлипидемия.
Въпрос
Коя е оптималната цел, препоръчана от повечето американски насоки за кръвното налягане на този пациент?
- 150/90 mmHg
- 140/90 mmHg
- 130/80 mmHg
- 120/80 mmHg
Верен отговор: 130/80 mmHg
Пациенти със съществуващи CVD, CKD и метаболитно заболяване са изложени на много висок риск от последващо CV събитие. Таргетно кръвно налягане от <130/80 mmHg е подходящо за пациенти, при които има висок CV риск, ако то може да бъде постигнато по безопасен начин.
Таргетите на кръвното налягане се основават главно върху риска за пациента от бъдещи CV събития. Насоките за лечение на диабет, кардиологични и бъбречни заболявания препоръчват лечение на хипертония при пациенти с висок риск от CV с таргетно кръвно налягане от <130/80 mmHg. Тази препоръка се основана върху доказателство, фаворизиращо интервенции или за бъбречна, или за CV протекция. По същия начин доказателството за интензивно понижение на кръвното налягане е най-силно за пациенти с висок абсолютен CV риск на входно ниво, който може да включва CVD, T2D и CKD.
Висок CV риск
Проучването SPRINT е включвало пациенти с висок CV риск и е оценявало дали таргетното лечение на систолно кръвно налягане BP (SBP) от <120 mmHg (интензивно лечение) е превъзхождало целта от <140 mmHg (стандартно лечение). Пациенти, при които 10-годишния CVD риск на входно ниво е бил ≥18%, са имали повече полза отколкото вреда от SBP таргет от <130 mmHg. От друга страна, SBP таргет от <140 mmHg е бил по-подходящ за тези, при които рискът на входно ниво е бил <18%. Пациентите, включени в проучването SPRINT, са имали ≥1 от следните рискови фактори: възраст ≥75години, клинично очевидно CVD, различно от удар, субклинично CVD (напр. повишен скор на калцификация на коронарната артерия чрез компютърно томографско сканиране, лява вентрикуларна хипертрофия или глезен-брахиален индекс <0.9), GFR от 20 до 59 mL/min/1.73 m2, или 10-годишен рисков скор на Фрамингам ≥15% (Комбинации от РФ повишаващи на риска за развитие на ССЗ за 10 години при наличието на 2 и повече РФ.).
Бъбречно заболяване
При пациенти с CKD, кохортна фаза от 4-годишното проучване AASK е оценила таргет за кръвно налягане от <130/80 mmHg при афроамериканци с хипертония. Рискът от прогресиране на CKD (определен като удвояване на серумния креатинин, ESRD, или смърт) се е понижил сигнификантно при пациенти с ACR на входно ниво>300 mg/дневно (HR 0.73; 95% CI: 0.58, 0.93). След завършване на кохортната фаза, участниците в AASK са били проследявани за междинен период от 14 години за краен стадий на бъбречно заболяване (end-stage renal disease – ESR) и смърт. Мета-анализ на дългосрочни, проследяващи данни, вкл. данните от AASK, също е демонстрирал по-ниска честота на прогресия при ESRD, специфично за пациенти с протеинуринно CKD. Обаче, дългосрочни ползи, свързани с преживяване са настъпили при пациенти с и без протеинурия. Общата смъртност се е понижила с 13% (HR 0.87, 95% CI: 0.76, 0.99).
В подгрупата CKD в SPRINT (N = 2646; средна eGFR = 48 mL/min/1.73 m2), която е постигнала интензивна цел на BP, е имало сигнификантно по-ниска смъртност от всякакво естество. Първоначалният смесен изход от MI, ACS, удар, сърдечна недостатъчност, или CV смърт, е бил също рядък и в групата с инвазивна цел. Все пак, резултатът е бил несигнификантен, вероятно, поради понижената статистическа вероятност за подгрупата с CKD. eGFR е била понижена в първите 6 месеца на проучването, предполагащо остър хемодинамичен ефект на ниско кръвно налягане, но е имало само лека разлика в понижението на eGFR между лекуваните групи след 6 месеца.
T2D
Интензивното понижение на кръвното налягане при пациенти с T2D е било отхвърлено по-рано от проучването ACCORD, което не постига първичния си MACE (Major Adverse Cardiac Events – неблагоприятни сърдечно-съдови събития) като резултат, въпреки че рискът от удар е бил значително понижен. ACCORD е използвал мултифакторен дизайн и хипертонията не е била единствената контролирана променлива. Пациентите са били рандомизирани също на интензивен или стандартен гюкозен контрол. Post-hoc анализ на данните от ACCORD показва, че интензивното кръвно налягане самостоятелно е подобрило основните CVD резултати. Последващи мета-анализи на проучвания също са подкрепили лечение към SBP таргет <130 mmHg, особено сред пациенти с T2D и SBP на входно ниво ≥140 mmHg.
Мета-анализ на над 100,000 участници в проучване съобщава, че за входно ниво на SBP ≥140 mmHg, всяко 10 mmHg по-ниско SBP е било свързвано със сигнификантно по-нисък относителен риск от смърт (13%), CV събития (11%), коронарно сърдечно заболяване (12%), удар (27%), албуминоурия (17%) и ретинопатия (13%). Обратното, когато SBP на входно ниво е било <140 mmHg, допълнителното понижение на SBP не се е свързвало с по-нисък риск от смърт, CV заболяване или събития на коронарна болест на сърцето; обаче, пациентите е вероятно да имат по-нисък риск от удар, ретинопатия и прогресия на албуминоурията. Екстраполираната полза от таргетно SBP <130 mmHg трябва да бъде балансирана с едновременните разходи и потенциални нежелани събития на допълнителни или по-високи дози за лечение.
Пациентът потвърждава, че взима Лозартан 100 mg, така като му е предписан. Съгласява се да започне комбинирани таблетки лозартан 100 mg/хидрохлоротиазид (HCTZ) 25 mg за по-нататъшно понижение на кръвното налягане. Споделеното внимание на лекаря се насочва наново върху другите му модифицируеми рискови фактори.
Въпрос
Кой следващо антидиабетично средство би добавил лекарят за постигане на масимална полза?
- Глюкагоно-подобен пептид -1 рецепторен (GLP-1 Ras)
- Прандиален инсулин
- Инхибитор на натриево-глюкозния котранспортер 2 (SGLT2)
- Не се прибавя друго антидиабетично средство
Верен отговор: Инхибитор на натриево-глюкозния котранспортер 2
Американската диабетна асоциация (ADA) и Европейската асоциация за изучаване на диабета (EASD) препоръчват всички пациенти с T2D и анамнеза за MI да се лекуват с SGLT2 инхибитор или GLP-1 RA, които са показали CV ползи. Макар и SGLT2 инхибитора или GLP-1 RA да са разумен избор на лечение, eGFR от 58 mL/min на пациента прави SGLT2 инхибитора малко по-подходящ. Добавянето на прандиален инсулин към настоящия режим с базален инсулин и 2 орални антидиабетични средства би помогнало за понижението на HbA1c , но с тенденция за наддаване на тегло и хипогликемични събития.
Въпрос
До каква степен HbA1c на пациента е повлияло лекарското решение? (Изберете от 1 [независимо от HbA1c] до 4 [основано изцяло върху HbA1c])
1 – решението е взето независимо от HbA1c
2
3
4 – решението се базира на HbA1c на пациента
Верен отговор: Решението е взето независимо от HbA1c
Насоките на ADA/EASD препоръчват решението за лечение на пациент с установено CVD с GLP-1 RA или SGLT2 инхибитор за понижение на MACE, хоспитализация за сърдечна недостатъчност, сърдечносъдова смърт или прогресия на CKD, да бъде обмислено независимо от HbA1c на входно ниво или индивидуализираното HbA1c.
Наскоро ADA/EASD актуализираха препоръките си за 2018 г. за лечение на хипергликемия, въз основа на важни находки от резултатите от големи CV проучвания (CVOTs), публикувани през 2019 г. Ако CKD (конкретно GFR ≥30 до ≤60 mL/min) или сърдечната недостатъчност (HF) преобладават, препоръката е за лечение с SGLT2 инхибитор с доказана CV полза, независимо от HbA1c на входно ниво. Ако преобладава атеросклеротична сърдечносъдова болест (ASCVD), препоръката е за лечение или с GLP-1 RA или с SGLT2 инхибитор с доказана CV полза, независимо от HbA1c на входно ниво.
Фиг 1. Алгоритъм на ADA/EASD за понижение на глюкозата при пациенти с ASCVD, CKD, или HF
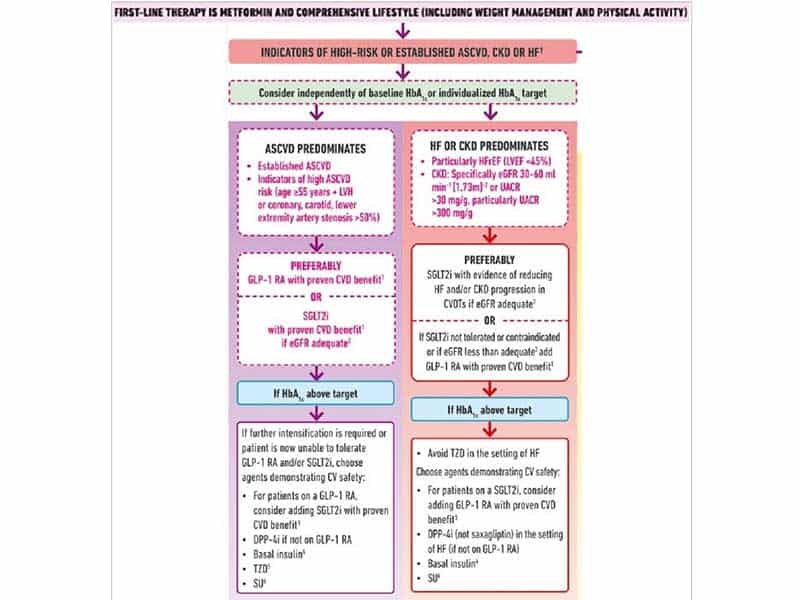
Действа, като се превръща в клинична предпоставка, независимо от съпътстващата глюкозопонижаваща терапия.
1. Доказана CVD полза означава, че има показана индикация за понижение на CVD събития.
2. Трябва да се има предвид, че показаната индикация SGLT2 инхибитор варира по региони и индивидуални агенти по отношение посоченото ниво на eGFR за започване и продължаване на употребата.
3. Емпаглифлозин, канаглифлозин и дапаглифлозин са показали понижение на HF и че понижават прогресията на CKD при CVOTs.
4. Деглудек и гларжин U100 са демонстрирали CVD безопасност.
5. Ниските дози може да се понасят по-добре, въпреки че са по-малко проучвани за CVD ефекти.
6. Избор на последно поколение SU за понижение риска от хипогликемия. Глимепирид е показал подобна CV безопасност в сравнение с DPP-4 инхибиторите.
SGLT2 iинхибиторите и GLP-1 RAs са понижили сигнификантно риска от големи CV събития (MACE) в неотдавнашни CVOTs, включващи пациенти с T2D, повечето от които са имали доказано CVD. (Taбл. 3.) SGLT2 инхибиторите емпаглифлозин, канаглифлозин и дапаглифлозин също са понижили риска от прогресия на бъбречно заболяване и хоспитализация за HF (HHF) в сравнение с плацебо. GLP-1 RA CVOTs не са идентифицирали повишение на риска от HHF.
Taбл. 3. Проучвания за проследяване на сърдечносъдовите крайни резултати (CVOTs) с SGLT2 инхибитори и GLP-1 RAs
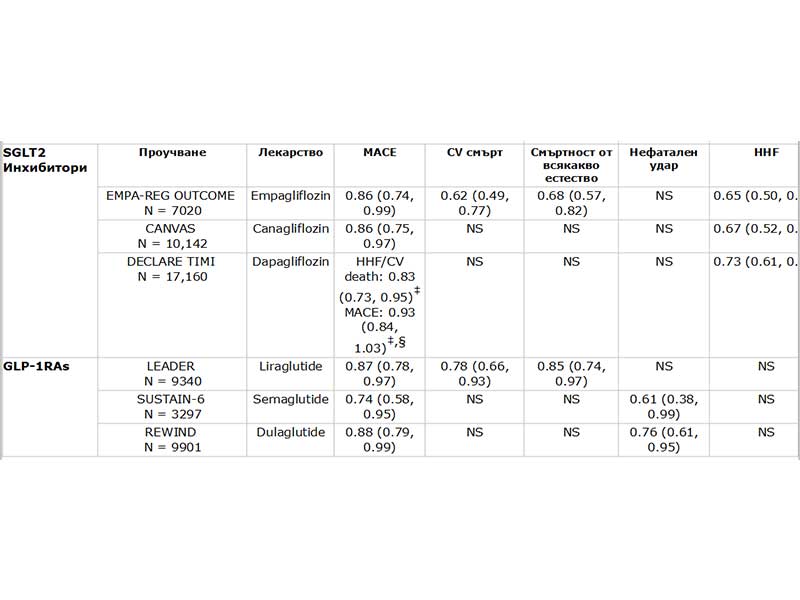
NS = не сигнификантно.
*Данни и съотношение на опасност (95% CI).
† бъбречна недостатъчност – резултатите са дефинирани по различен начин при отделните CVOT, но най-често включват вариация на трайно нарастване на макроалбуминурията, нефрологина заместителна терапия, удвояване на серумния креатинин (sCr) или >30% намаление на eGFR, ESRD или смърт от бъбречно заболяване.
‡Резултатите от първоначалната ефикасност са били MACE и предпоставка за CV смърт или HHF.
§P< .001 за не превъзхождане.
CVOTs с SGLT2 инхибитори са показали постоянна полза за бъбреците, но са били също оценени като вторични резултати в проучвания, разработени първоначално за оценка на CV безопасността. Наскоро, посветените проучвания на бъбречните функции CREDENCE (канаглифлозин) и DAPA-CKD (дапаглифлозин) са били завършени за класа SGLT2 инхибитор. Пациентите, включени в CREDENCE, са имали T2D с HbA1c от 6.5% до 12%, eGFR 30 до <90 mL/min/1.73 m2 и екскреция на албумин >300 mg/g. Всички са били лекувани с максимално поносимата доза ACE инхибитор или ARB. При половината от пациентите е било доказано CVD. Канаглифлозин 100 mg е понижил сигнификантно риска от първична предпоставка, допринасяща за достигане на ESRD, удвоил е серумния креатинин и CV или бъбречната смърт (HR: 0.70 [N = 4401; 95% CI: 0.59, 0.82]). В DAPA-CKD, пациенти с или без диабет са имали eGFR ≥25 и ≤75 mL/min/1.73 m2, екскреция на албумин ≥200 mg/g и са били на максимално поносима доза от ACE инхибитор или ARB. Дапаглифлозин е понижил първичната предпоставка за достигане на крайна степен на влошаване на бъбречните функции, CV или бъбречна смърт с 39% (HR: 0.61 N = 4304; 95% CI: 0.51, 0.72), с редукции от 36% и 50% съответно при пациенти с и без T2DM. Емпаглифлозин 45 mL/min/1.73 m2; канаглифлозин не се препоръчва при eGFR <30 m/min/1.73 m2.
Няма все още публикувано GLP-1 RA проучване, което да дава оценка на основните показатели за бъбречната функция като първична крайна точка. Неотдавнашен мета-анализ на вторични или проучвани функционални бъбречни резултати от GLP-1 RA CVOTs показва, че GLP-1 RAs се свързват с 17% редукция на относителния риск от влошаване на основните показатели за бъбречната функция, включващи развитието на макроалбуминоурия, удвояването на серумния креатинин или понижението на eGFR с ≥40%, бъбречно-заместителна терапия и бъбречна смърт (HR 0.83; 95% CI: 0.78, 0.89; P < .0001).[30]
Пациентът се съгласява да добави SGLT2 инхибитор към текущото си лечение.
Въпрос
Кое от следните изброени би казал лекарят на пациента на инсулин, който започва прием на SGLT2 инхибитор?
- Изпреварващата редукция на инсулина ще понижи по безопасен начин риска от кетоза
- Временно спиране на SGLT2 инхибитор, ако претърпява планирана операция
- Визита след 4 седмици за проверка нивото на калия
- Изследване всяка сутрин на урината за кетоза
Верен отговор: Временно спиране на SGLT2 инхибитор, ако претърпява планирана операция
Едновременната употреба на инсулин или сулфонилурея (SU) повишава риска от хипогликемия с SGLT2 инхибиторите, особено рано след започването. Обаче, изпреварващите съществени редукции на дозата инсулин могат да ускорят еугликемичната диабетна кетоацидоза (DKA). Еугликемичната DKA е рядък, но сериозен нежелан ефект от SGLT2 инхибиторите. Инсулинозависимите пациенти трябва да понижат дозата инсулин колкото е нужно и да се посъветват временно да преустановят SGLT2 инхибитора, ако претърпяват планирана операция. Не е нужно рутинно мониториране за кетони при пациенти с T2D.
През 2015 г. FDA актуализира всички предписания за SGLT2 инхибиторите с предупреждение за повишен риск еугликемичната диабетна кетоацидоза (DKA). В популационно базирано кохортно проучване е наблюдавано, че при SGLT2 инхибиторите е имало почти 3 пъти повишение на риска от DKA (HR: 2.85; CI: 1.99, 4.08). DKA, свързана с SGLT2 инхибитора, е нечеста (~0.5 пациент-годишно/1000 пациент-годишно), но връзката й с еугликемичните глюкозни нива < 250 mg/dL е атипична за проява на DKA и е по-лесно пренебрегвана. През 2020 FDA одобрява допълнителни промени в информацията за предписване за всички SGLT2 инхибитори като препоръчва те да се спрат временно 3 – 4 дни преди планирана операция, за да се намали риска от DKA. Може да се възобнови приема на SGLT2 инхибитор веднага щом оралния прием на пациента е станал отново такъв, какъвто е бил на входно ниво и са разрешени всякакви други рискови фактори за кетоацидоза.
Рискът от DKA може да се повиши при инсулинозависими пациенти или латентен автоимунен диабет с бърза еволюция към диабет тип 1. Когато инсулинозависими пациенти започват прием на SGLT2 инхибитор, те трябва да мониторират внимателно кръвната глюкоза (BG). Дозата инсулин трябва да се понижи, ако BG спадне по-ниско от таргетното ниво или се развие хипогликемия. Обаче, по-ниската доза инсулин може да е недостатъчна за потискане на кетогенезата и риска при пациента от DKA може да се повиши.
Пациентите трябва да се информират за ситуациите, които могат да ускорят DKA и за симптомите на DKA. (Taбл. 4) Допълнителни практически съображения за употребата на SGLT2 инхибиторите са изброени също в Taбл. 4.
Taбл. 4. Практически съображения за употреба на SGLT2 инхибитори


Заключение
Пациентът се явява на проследяваща визита след 3 месеца. Лекарят го информира радостно, че неговото HbA1c спаднало до 6.8%, а BP е 130/85 mmHg. „Вие успяхте успешно да понижите риска от нов сърдечен удар,“, поздравява го той. Пациентът се усмихва широко и казва „Точно това исках да чуя.“






