
Брой 9/2010
Доц. д-р Тошо Балабански,
Университетска национална кардиологична болница, София
Внезапната сърдечна смърт настъпва чрез следните механизми: камерно мъждене – 62.4%; брадиаритмии – 16.5%; torsades de pointes – 12.7%; камерна тахикардия – 8.3%1. Това означава, че над 80% от случаите на внезапна сърдечна смърт се дължат на камерни тахиаритмии.
Видове камерни тахиаритмии
Оценката на всяка камерна тахиаритмия включва ЕКГ, хемодинамика и подлежащо заболяване.
Според ЕКГ камерните аритмии се делят на:
– непродължителна камерна тахикардия (мономорфна или полиморфна);
– продължителна камерна тахикардия (мономорфна или полиморфна);
– камерна риентри;
– тахикардия в проводните бедра;
– камерна тахикардия в две посоки, torsades de pointes;
– камерно трептене/мъждене (Фиг. 1)
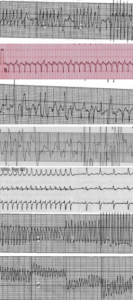
Фигура 1 Отгоре надолу:
– непродължителна камерна тахикардия (мономорфна);
– продължителна камерна тахикардия (мономорфна);
– продължителна камерна тахикардия (полиморфна);
– камерна тахикардия в две посоки;
– камерна риентри тахикардия в проводните бедра;
– камерно трептене, камерно мъждене.
Според хемодинамиката камерните тахиаритмии се делят на два вида.
Тези, които са със стабилна хемодинамика, обикновено протичат без симптоматика или с палпитации.
Нестабилната хемодинамика води до по-сериозна клинична изява – пре-синкоп (световъртеж, замайване и много лесна умора), синкоп, сърдечен арест и внезапна сърдечна смърт.
Камерните тахиаритмии са свързани най-често със следните подлежащи заболявания и състояния:
– ИБС;
– вроден сърдечен порок;
– кардиомиопатия (дилатативна, хипертрофична, аритмогенна деснокамерна);
– сърдечна недостатъчност;
– неврологични заболявания.
Възможна е изява на камерна тахикардия и при структурно здраво сърце.
ВНЕЗАПНА СЪРДЕЧНА СМЪРТ
Изследвания
Необходимите изследвания след преживян сърдечен арест са следните: ЕКГ, работна ЕКГ проба, холтер ЕКГ, специфични ЕКГ изследвания за аритмия, ехокардиография, оценка на лявокамерна функция, оценка за коронарно-съдова болест, електрофизиологично изследване.
Електрокардиограмата е първо и задължително изследване, като установяването на патологично отклонение насочва към последващите изследвания.
Работна ЕКГ проба се провежда при пациенти с:
– умерена или висока вероятност за ИБС според възраст, пол и симптоматика;
– регистрирани или подозирани камерни аритмии, провокирани от физически усилия.
Холтер ЕКГ се провежда с оглед установяване на камерна аритмия, промени в QT-интервала, алтернанс на T-вълната, СТ-промени. При наличие на спорадична симптоматика е уместно да се извърши дългосрочно мониториране чрез съответно устройство за имплантиране или за активиране от страна на болния при наличие на субективни оплаквания.
Специфичните ЕКГ изследвания за аритмия включват изследване на:
– алтернанс на Т-вълната;
– вариабилност на сърдечната честота;
– турбуленция на сърдечната честота;
– барорефлексна чувствителност,
– сигнално осреднена ЕКГ.
Те могат да подобрят оценката на риска за настъпване на камерна тахиаритмия.
Ехокардиографията има висока диагностична стойност при кардиомиопатия, хипертония с умерена и тежка лявокамерна хипертрофия, клапно сърдечно заболяване и преживян миокарден инфаркт.
Стрес-ехография или позитронна-емисионна компютърна томография (SPECT) се налага при необходимост от допълнителна оценка на лявокамерната функция или при съмнение за подлежаща тиха исхемия при пациенти с умерена вероятност за ИБС. Тези изследвания имат добра диагностична стойност в случаи, когато работната ЕКГ проба е по-малко информативна (терапия с дигоксин, лявокамерна хипертрофия и СТ-депресия над 1 мм в покой, WPW-синдром, ляв бедрен блок). Алтернативно и по клинична преценка може да се проведат ядрен магнитен резонанс или компютърна томография.
Честотата на внезапната сърдечна смърт е най-висока при ИБС, особено след преживян миокарден инфаркт. При клинично съмнение за ИБС се налага често провеждане на селективна коронарография с последващо стентиране на коронарните съдове. Реваскуларизацията на коронарните съдове има решаващо значение в лечението на камерните тахиаритмии.
Библиография
1. Zipes DP. Epidemiology and mechanisms of sudden cardiac death. Can J Cardiol 2005; 21 (Suppl A):37A-40A.
2. Moss AJ, Zareba W, Hall J et al. Prophylactic implantation of a defibrillator in patients with myocardial infarction and reduced ejection fraction. N Engl J Med 2002;346:877-883.
3. Packer DL, Prutkin JM, Hellkamp AS, et al. Impact of implantable cardioverter-defibrillator, amiodarone, and placebo on the mode of death in stable patients with heart failure. Analysis from the Sudden Cardiac Death in Heart Failure Trial. Circulation 2009; 120(22):2170-6.
4. Anderson JL, Hallstrom AP, Epstein AE, Pinski SL, Rosenberg Y, Nora MO, Chilson D, Cannom DS, Moore R. Design and Results of the Antiarrhythmics vs Implantable Defibrillators (AVID) Registry. Circulation. 1999;99:1692-1699.
5. Kuck KH, Cappato R, Siebels J, Rüppel R. Randomized comparison of antiarrhythmic drug therapy with implantable defibrillators in patients resuscitated from cardiac arrest : the Cardiac Arrest Study Hamburg (CASH). Circulation. Aug 15 2000;102(7):748-54.
6. Multicenter Automatic Defibrillator Implantation Trial (MADIT): design and clinical protocol. PACE 1991, 14:920-927.
7. Buxton AE, Lee KL, Fisher JD, Josephson ME, Prystowsky EN, Hafley G. A randomized study of the prevention of sudden death in patients with coronary artery disease. Multicenter Unsustained Tachycardia Trial Investigators. N Engl J Med. 1999;341:1882-1890.






