
Брой 9/2011
Д -р А. Александров, д-р Ст. Иванов,
доц. Д. Гочев
Клиника по кардиология и ревматология, ВМА-София
Внезапната сърдечна смърт (ВСС) се дефинира като естествена смърт, резултат на кардиачни причини, изявена с остра загуба на съзнание в рамките на един час от началото на острите симптоми; съществуването на предшестващата сърдечна болест може да бъде известно, но времето и началото на настъпване на смъртта са неочаквани (1). Терминът „неочаквани” е отличителен белег на дефиницията, защото той позволява включването на голяма група предхождащи състояния, имащи различни нива на риск (2).
Трудно е да се определи честотата на ВСС в световен мащаб, тъй като тя варира съществено в зависимост от преобладаването на исхемичната болест на сърцето в различните държави. Честотата на ВСС в САЩ е 0.1-0.2% за година за населението >35 години. Честотата в Европа е сходна с тази в САЩ (2).
ВСС е голям обществен здравен проблем. Честотата на ВСС в САЩ е 400 000/година. Въпреки напредъка в ресусцитацията лечението на ВСС обикновено е неуспешно и с малки изключения по-голямата част от пациентите, преживели сърдечен арест, не оцеляват (3).
Придобити клапни пороци и ВСС
Клапните пороци не са водеща причина за ВСС, но относително високата им честота повишава тяхното значение като причина за настъпване на ВСС. В един патологоанатомичен регистър, обхващащ 1000 човека на възраст под 65 години без предшестващо сърдечно заболяване, се установило, че клапните болести на сърцето са четвъртата причина за внезапна сърдечна смърт след коронарната болест на сърцето, кардиомиопатиите и уврежданията в проводната система на сърцето (4). Дори клапните болести на сърцето да са отговорни за малка част от случаите на ВСС, относително високата честота на клапните пороци повишава тяхното значение като причина за настъпване на ВСС (5).
Клапните пороци на сърцето може да бъдат ефективно лекувани чрез хирургични интервенции и затова е особено важно да се определят подгрупи от пациенти, които са с повишен риск от ВСС, при които да се предприеме по-агресивна стратегия. Развитието на симптоми на сърдечна недостатъчност и белези на левокамерна систолна дисфункция са предиктори на повишен риск от ВСС и затова са сигурни показания за хирургично лечение. Трябва да се отбележи, че данните в литературата относно ВСС при пациенти с клапни болести на сърцето са доста по-ограничени в сравнение с тези за исхемичната болест на сърцето и кардиомиопатиите.
Аортна стеноза
Аортната стеноза е най-често срещаният клапен порок в Европа и Северна Америка и честотата му се увеличава със застаряването на населението. Най-честата причина за развитие на аортна клапна стеноза е калцификацията на аортната клапа при възрастни пациенти (2-7% от хората на възраст >65 години), на второ място се нарежда вродената аортна клапна стеноза, тя се среща в по-ранна възраст. Ревматичната аортна стеноза става все по-рядка (6, 7).
Високостепенната аортна клапна стеноза е отговорна за немалък брой случаи на ВСС, главно при възрастни хора. Според различните източници смъртта при пациентите с аортна стеноза настъпва внезапно в 20 до 50% от случаите (8, 9). За съжаление не съществува инструментален или клиничен параметър, който да позволява определянето на пациентите с аортна стеноза, които са с най-висок риск за ВСС. Аортното клапно протезиране, което се препоръчва при всички симптоматични пациенти, съществено намалява риска от ВСС (8).
Патогенеза на ВСС при аортна клапна стеноза
Причината за ВСС при пациентите с аортна клапна стеноза е трудно да се определи и причините най-често са много. Те може да бъдат групирани по следния начин:
нарушение на барорецепторния механизъм
камерна аритмия, предизвикана от исхемия на миокарда (която при аортна стеноза е налице дори без да има коронарна болест)
атриовентрикуларен блок в резултат на тежка аортна клапна калцификация, която засяга проводната система на сърцето.
Симптоматични пациенти с аортна стеноза
Развитието на симптоми при пациенти с аортна стеноза е ключов момент в развитието на заболяването. При пациентите с високостепенна аортна стеноза 50-процентната преживяемост е 5 години при изява на стенокардия, 3 години при синкоп и 2 години при изява на задух или застойна сърдечна недостатъчност. Поради това при симптоматичните пациенти с високостепенна аортна клапна стеноза трябва да се извърши аортно клапно протезиране без излишно отлагане на операцията.
Асимптоматични пациенти с аортна стеноза
Резултатите от редица проспективни проучвания показват, че честотата на ВСС при асимптоматични пациенти с високостепенна аортна стеноза е под 1% (10, 11). Рискът от усложнения, свързани с аортното клапно протезиране, е по-висок от риска от ВСС при тези пациенти, поради което не се препоръчва клапно протезиране на всички асимптомни пациенти с аортна стеноза с цел превенция на ВСС (5). Съществува обаче високорискова подгрупа пациенти с асимптоматична високостепенна аортна клапна стеноза. Установили са критерии, свързани с повишен риск от развитие на симптоми и необходимост от аортно клапно протезиране (5). Тези критерии включват:
1. Тежест на стенозата. Предиктори на лоша прогноза са:
– пикова скорост на аортния кръвоток ≥4 m/s;
– бързо увеличаване на скоростта на аортния кръвоток ≥0,3 m/s за година (12, 13);
– площ на аортната клапа
2. Тест с натоварване. Наличието на аортна стеноза, дори умерена, традиционно е считано като противопоказание за извършване на тест с натоварване. Такъв тест не трябва да се извършва само при симптоматични пациенти. При асимптоматични пациенти тестът с натоварване е информативен и безопасен, когато се провежда под строг медицински контрол (15). По време на теста може да се изявят симптоми при пациенти, които до този момент не са имали такива, и това може да осигури важна прогностична информация.
3. Калцификация на аортната клапа. Калцификацията на аортната клапа е процес, който води до развитие на аортна клапна стеноза. Степента на калцификация осигурява важна прогностична информация (16). Установено е, че умерената и тежката калцификация на клапата, оценени ехокардиографски или компютъртомографски, са свързани с лоша прогноза за пациента (17).
4. Коронарна артериална болест. Установено е 50% увеличаване на сърдечната смъртност в резултат на миокарден инфаркт при пациенти с аортна стеноза, което предполага връзка между аортната клапна болест и коронарната артериална болест (18). При пациентите с лека или умерена аортна стеноза наличието на коронарна артериална болест е независим предиктор на прогнозата (фиг. 1).
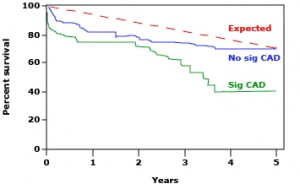
Фиг. 1. Каплан-Майеровата крива на преживяемост при пациенти със и без ИБС, претърпели аортно клапно протезиране по повод аортна стеноза. Установява се, че пациентите с аортна клапна стеноза и левокамерна систолна дисфункция, които нямат исхемична болест на сърцето (ИБС), имат преживяемост, близка до очакваната за общата популация. Преживяемостта е значително по-ниска при наличие на ИБС (19)
Показания за аортно клапно протезиране при асимптомни пациенти с високостепенна аортна клапна стеноза – Европейско кардиологично общество (20)
Аортно клапно протезиране трябва да се извърши при:
1. Пациенти с абнормен отговор по време на физическо натоварване – изява на симптоми (IC), понижаване на артериалното налягане, неадекватно повишаване на артериалното налягане (IIaC), значително редуциран физически капацитет.
2. Пациенти с левокамерна дисфункция (фракция на изтласкване <50%) (IC). 3. Пациенти, на които им предстои аорто-коронарен байпас, операция на асцендентната аорта или на друга клапа (IC). Пациенти с умерена аортна стеноза, на които им предстои аорто-коронарен байпас, операция на асцендентната аорта или на друга клапа, също са показани за аортно клапно протезиране (IIaC). 4. Пациенти с умерена до тежка калцификация, пикова скорост на аортния кръвоток >4 m/s или при бързо увеличаване на пиковата скорост (≥ 0,3 m/s за година) (IIaC).
5. Пациенти с градиент
Аортно клапно протезиране може да се обсъжда и при:
1. Тежка левокамерна хипертрофия (дебелина на стените >15mm), освен ако не се дължи на артериална хипертония (IIbC).
2. Наличие на животозастрашаващи камерни аритмии по време на теста с натоварване, за които не може да се установи друга причина освен високостепенната аортна стеноза (IIbC).
3. Пациенти с градиент
Аортна инсуфициенция
Аортната инсуфициенция се дължи на неплътното затваряне на аортните клапни платна по време на диастола, в резултат на което част от левокамерния ударен обем се връща от аортата обратно в лявата камера. Допълнителният обем кръв, който се връща в лявата камера, води до повишаване на левокамерния теледиастолен обем и повишаване на стреса на левокамерната стена. Аортната инсуфициенция може да се раздели на остра и хронична.
Пациенти с високостепенна симптоматична аортна инсуфициенция
Появата на симптоми при пациентите с високостепенна аортна инсуфициенция е голям независим прогностичен фактор за ВСС (21, 22). Ако не се извърши аортно клапно протезиране, прогнозата на такива пациенти е лоша. Смъртността при тези, които не са се оперирали, е 24-25% годишно (21). Затова такива пациенти трябва да бъдат незабавно насочвани за оперативно лечение (10, 11). Пациенти с високостепенна аортна инсуфициенция, които предоперативно имат прояви на сърдечна недостатъчност III и IV ФК по NYHA, имат по-ниска преживяемост в сравнение с тези с I и II ФК (фиг. 2). Навременното извършване на операцията, когато заболяването не е напреднало, води до отлични далечни резултати (22).
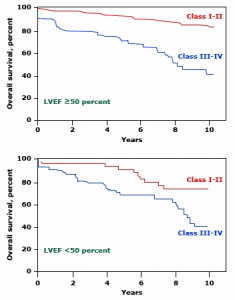
Фиг. 2. Пациенти с високостепенна аортна инсуфициенция, които предоперативно имат прояви на сърдечна недостатъчност III и IV ФК по NYHA, имат по-малка преживяемост в сравнение с тези с I и II ФК независимо дали левокамерната ФИ е ≥50% или е <50% (22)
Асимптоматични пациенти с високостепенна аортна инсуфициенция
Метаанализ установява, че рискът от ВСС при асимптоматичните пациенти с високостепенна аортна инсуфициенция е нисък (<0,2% годишно) (23, 24). Трябва да се отбележи, че има някои подгрупи от пациенти, които са с по-висок риск от ВСС. Прогнозата на асимптоматичните пациенти с високостепенна аортна инсуфициенция се определя от левокамерните размери и функция. Левокамерната дилатация и систолна дисфункция са свързани с по-висока честота на ВСС. Левокамерен теледиастолен размер (ЛКТДР) >70 мм и/или левокамерен телесистолен размер (ЛКТСР) >55 мм (според някои автори >50 мм) и ФИ <45% (според някои автори <50%) са свързани с по-висок риск от ВСС. Наличието на съпътстваща високостепенна митрална инсуфициенция е допълнителен индикатор за намалена преживяемост и повишен риск от ВСС. Показания за аортно клапно протезиране при асимптомни пациенти с високостепенна аортна инсуфициенция – Европейско кардиологично общество (20) Аортно клапно протезиране трябва да се извърши при: 1. При ФИ в покой ≤50% (IB) 2. При пациенти, на които им предстои извършване на аорто-коронарен байпас или операция на асцендентната аорта или на друга сърдечна клапа (IC). 3. При ФИ >50% и високостепенна дилатация на лявата камера – ЛКТДР >70 мм (75 мм според АСС/АНА) или ЛКТСР >50 мм (55 мм според АСС/АНА) или >25 мм/м2 телесна площ (IIaC).
4. При дилатация на аортния корен независимо от степента на аортната инсуфициенция или левокамерната функция при:
а) размер на аортния корен >55 мм при пациенти с трикуспидна аортна клапа (IIaC);
б) размер на аортния корен >50 мм при пациенти с бикуспидна аортна клапа; (може да се извърши и клапно съхраняваща операция) (IIaC);
в) размер на аортния корен >45 мм при пациенти със синдром на Marfan (може да се извърши и клапно съхраняваща операция) (IC).
В случаите на дилатация на аортния корен, посочени в т. 4, се извършва протезиране на асцендентната аорта. Аортно клапно протезиране не е показано при асимптоматични пациенти с високостепенна аортна инсуфициенция, които имат запазена систолна функция (ФИ >50%) и нямат левокамерна дилатация.
Остра аортна инсуфициенция
Острата аортна инсуфициенция е спешно състояние в медицината и е свързана с висок риск от ВСС. Това се дължи на неспособността на лявата камера да се адаптира към бързо повишаващия се теледиастолен обем, който се получава от големия обем кръв (регургитационния обем), който се връща в лявата камера по време на диастола в резултат на недоброто затваряне на аортната клапа. Ако не се коригира хирургично, острата аортна инсуфициенция често води до развитието на кардиогенен шок.
Основните причини, които може да доведат до развитието на остра аортна инсуфициенция, са: ендокардит и дисекация на аортата.
Лечение
Лечението на острата високостепенна аортна инсуфициенция е аортно клапно протезиране, което се извършва в спешен порядък. Ако хирургичната интервенция не може да се извърши веднага, може да се направи опит за стабилизиране състоянието на пациента в интензивно отделение с помощта на интравенозни вазодилататори като нитропрусид и инотропни агенти като допамин или добутамин в опит да се поддържа относително добър сърдечен дебит при по-ниско левокамерно теледиастолно налягане. Поставянето на интрааортен контрапулсатор е противопоказно, тъй като раздуването на балона по време на диастола ще влоши аортната инсуфициенция. Обемът на хирургичната интервенция зависи от причината за острата аортна инсуфициенция, като варира от аортно клапно протезиране и протезиране на асцендентната аорта при аортна дисекация до пластика на аортната клапа при руптура на фенестрирано аортно клапно платно.
Митрална инсуфициенция
Митралната инсуфициенция е често срещана клапна увреда, която може да възникне вследствие на увреда във всяка част от митралния клапен апарат. Той включва: клапни платна, клапен пръстен, хорди (chordae tendineae) и папиларни мускули. Левопредсърдната стена и левокамерният миокард, за който са заловени папиларните мускули, са също интегрално включени във функцията на митралната клапа. Честотата на митралната инсуфициенция се увеличава през последните години, което се дължи на застаряването на населението и високата честота на дегенеративните лезии сред възрастните.
Хронична митрална инсуфициенция
Пациенти със симптоматична високостепенна митрална инсуфициенция
Пациентите със симптоматична високостепенна митрална инсуфициенция са с по-висок риск от ВСС в сравнение с тези без прояви на сърдечна недостатъчност. Пациентите с високостепенна митрална инсуфициенция и прояви на сърдечна недостатъчност III и IV ФК по NYHA имат повишена смъртност, ако се лекуват консервативно (25), оперативното лечение при тези пациенти също е свързано с по-висока смъртност (фиг. 3) (26). При симптоматичните пациенти с високостепенна митрална инсуфициенция трябва да се извърши митрално клапно протезиране независимо от фракцията на изтласкване.
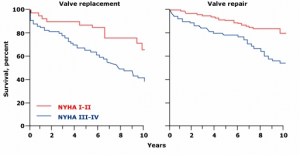
Фиг. 3. Преживяемост след митрално клапно протезиране/пластика на митралната клапа при симптоматични пациенти с високостепенна митрална инсуфициенция. Преживяемостта е по-добра при пациентите с прояви на сърдечна недостатъчност I и II ФК по NYHA в сравнение с тези с III и IV ФК, без значение дали се извършва пластика или протезиране на митралната клапа (26)
Пациенти с асимптоматична високостепенна митрална инсуфициенция
Честота и предиктори на ВСС
ВСС може да настъпи и при асимптомни пациенти с високостепенна митрална инсуфициенция. Независими детерминанти за настъпване на ВСС при тези пациенти са:
– левокамерната ФИ;
– функционалният клас по NYHA;
– наличието на предсърдно мъждене.
Честотата на ВСС е значително по-висока при пациенти с високостепенна митрална инсуфициенция и ФИ <50% в сравнение с тези с ФИ >50%. ВСС настъпва по-често и при пациентите с предсърдно мъждене в сравнение с тези, които са в синусов ритъм (27).
Не съществуват рандомизирани клинични проучвания, които да сравняват резултатите от ранното хирургично лечение с тези от медикаментозното лечение при асимптомните пациенти. Установено е, че ако митралното клапно протезиране се извърши при пациенти с високостепенна митрална инсуфициенция при запазена ФИ и СН I или II ФК по NYHA, намалява честотата на ВСС и преживяемостта е сходна с очакваната за съответната популация (26).
Препоръки за хирургично лечение при асимптомни пациенти с високостепенна митрална инсуфициенция – Европейско кардиологично общество (20)
Митрално клапно протезиране трябва да се извърши при:
1. Белези на левокамерна дисфункция (ФИ<60% и/или ЛКТСР >45 mm) (IC).
2. Запазена левокамерна систолна функция и предсърдно мъждене или налична пулмонална хипертония (систолно налягане в покой в a. pulmonalis >50 mmHg) (IIaC).
3. Тежка левокамерна систолна дисфункция (ЛК ФИ <30% и/или ЛКТСР >55 mm), рефрактерна на медикаментозна терапия при висока вероятност за пластика на МК и нисък оперативен риск (IIaC).
4. При липса на белези на левокамерна дисфункция хирургична корекция може да се извърши при висока вероятност за пластика на митрална клапа при нисък оперативен риск (IIbB).
5. Пациенти с тежка левокамерна дисфункция (ЛК ФИ <30% и/или ЛКТСР >55mm), рефрактерна на медикаментозна терапия при ниска вероятност за пластика (IIbC).
Остра митрална инсуфициенция
Острата митрална инсуфициенция е едно от спешните състояния в кардиологията, което е свързано със сериозни хемодинамични промени и изисква неотложно медикаментозно или хирургично лечение.
Съществуват три основни механизма, които може да доведат до развитие на остра митрална инсуфициенция на нативна клапа:
Вършеещо митрално платно (mitral flail leaflet), дължащо се на миксоматозна болест (митрален клапен пролапс), инфекциозен ендокардит или травма.
Руптура на chordae tendineae, спонтанна руптура, инфекциозен ендокардит или остър ревматизъм.
Руптура на папиларен мускул или папиларномускулна дисфункция в резултат на остър миокарден инфаркт, тежка исхемия или травма.
Дефинитивното лечение на острата митрална инсуфициенция в повечето случаи е оперативно. Медикаментозно лечение може да бъде необходимо по време на диагностицирането на състоянието и до извършването на оперативното лечение.
Пролапс на митралната клапа
Митралният клапен пролапс е често срещана клапна увреда в общата популация (между 0.6 и 2.4%) (28, 29). Основни детерминанти на ВСС при хората с митрален клапен пролапс са:
– функционалният клас по NYHA и наличието на предсърдно мъждене (27). При пациентите с пролапс на митралната клапа показателите, свързани с повишен риск, включват също: наличие на умерена или високостепенна митрална инсуфициенция, левокамерна ФИ под 50%, увеличен левопредсърден или левокамерен размер, предсърдно мъждене, вършеещо митрално клапно платно и възраст ≥50 години (30, 31). Честотата на ВСС е значително по-висока при пациентите с т. нар. „вършеещо митрално платно” (flail mitral leaflet), особено при тези, които се лекуват консервативно.
– Повишен риск от ВСС при пациентите с пролапс на митралната клапа е налице при: анамнеза за синкоп или пресинкоп, особено ако има документирана аритмия, симптоматика (палпитации, гръдна болка, задух); удължен QT интервал или реполаризационни промени в долнолатералните отвеждания, чести или комплексни камерни екстрасистоли, пролапс на предно и задно митрално платно, фамилна анамнеза за свързана с митралния клапен пролапс ВСС (32).
Лечение
Пациентите с пролапс на митралната клапа, които са преживели сърдечен арест или продължителна камерна тахикардия, са показани за имплантиране на кардиовертер дефибрилатор (ICD). Оперативна корекция на митралния клапен пролапс се налага само при определени пациенти с високостепенна митрална инсуфициенция. Критериите за оперативно лечение са същите, както и за пациентите с високостепенна хронична митрална инсуфициенция.
Митрална стеноза
Ревматичната митрална стеноза е с голяма честота в развиващите се държави (7). Основните причини за настъпване на фатален изход при пациентите, които не се лекуват, са: застойната сърдечна недостатъчност или белодробният оток, тромбемболичните инциденти и инфекциите. При пациентите с митрална стеноза не се установява повишена честота на ВСС, като вероятно това се дължи на факта, че при чистата митрална стеноза не настъпва ремоделиране на ЛК.
Артериална хипертония и ВСС
Артериалната хипертония е един от доказаните рискови фактори за ИБС и е един от значимите рискови фактори за ВСС (33). Една от първите патофизиологични последици от дългогодишната артериална хипертония е развитието на левокамерна хипертрофия. Наличието на левокамерна хипертрофия е свързано с повишаване честотата на сърдечната недостатъчност, камерната екстрасистолна аритмия, миокардния инфаркт, намалената левокамерна фракция на изтласкване, ВСС, общата смъртност, дилатацията на аортния корен и мозъчносъдовите инциденти. Левокамерната хипертрофия е свързана също с повишен риск от сърдечносъдови инциденти (нестабилна стенокардия, инфаркт на миокарда, сърдечна недостатъчност, камерна екстрасистолна аритмия), инсулт, сърдечносъдова смъртност (76-82). Увеличаването на левокамерната маса е пряко свързано с нарастване на сърдечносъдовия риск (фиг. 4 и 5) (34, 35).
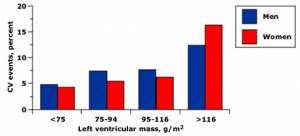
Фиг. 4. Честота на сърдечносъдовите инциденти при проследяване в продължение на 4 години на мъже и жени с различна левокамерна маса, участващи във Фрамингамското проучване. Пациентите са разделени на няколко групи в зависимост от левокамерната маса, определена ехокардиографски. Пациентите с по-голяма левокамерна маса имат повишена честота на сърдечносъдовите инциденти (34)
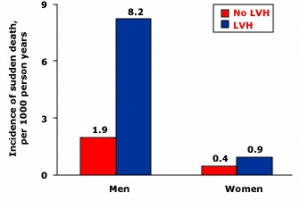
Фиг. 5. Честота на ВСС при жени и мъже със и без левокамерна хипертрофия. Честотата на ВСС е свързана с наличието и степента на левокамерната хипертрофия. Както при мъжете, така и при жените наличието на левокамерна хипертрофия повишава риска от ВСС (35)
Механизми, отговорни за повишения риск от ВСС при пациенти с левокамерна хипертрофия
Повишеният сърдечносъдов риск, свързан с левокамерната хипертрофия, се дължи до голяма степен на исхемията на миокарда. Левокамерната хипертрофия предизвиква също редица електрофизиологични промени, които са свързани с повишено предразположение към предсърдно мъждене, камерни екстрасистолни аритмии, особено torsades de pointes и ВСС. Нарушената вътрекамерна проводимост, която се наблюдава при част от пациентите с левокамерна хипертрофия, е свързана с повишен риск от ВСС (1).
Артериосклеротичните аневризми на абдоминалната аорта и аортните дисекации може да настъпят при пациенти с хронична хипертония. При хипертониците може да настъпят мозъчни инфаркти. При дългогодишна хипертония и лош контрол на АН може да настъпи руптура на аневризма на интракраниална артерия, най-често във Вилизиевия кръг, в резултат на което да настъпи ВСС.
Ефект на антихипертензивната терапия
Понижаването на артериалното налягане с антихипертензивни медикаменти, редукцията на телесната маса и намаленият прием на натриев хлорид водят до намаляване на левокамерната маса, което води до понижаване на сърдечносъдовия риск.
По-бърза регресия на левокамерната хипертрофия се наблюдава след лечение в продължение на няколко месеца с АСЕ инхибитори, ангиотензин рецепторни блокери (АРБ), директния ренинов инхибитор aliskiren, някои от калциевите антагонисти (дилтиазем, верапамил и амлодипин), както и с някои от симпатиколитичните медикаменти (methyldopa и алфа-блокерите) (36). Намаляването на левокамерната хипертрофия води до намаляване на сърдечносъдовия риск.
От друга страна, намаляването на левокамерната хипертрофия е по-слабо изразено при лечение с диуретици и бета-блокери и липсва при директните вазодилататори (като hydralazine или minoxidil) и някои калциеви антагонисти въпреки адекватния контрол на артериалното налягане. Липсата на ефективност по отношение на левокамерната хипертрофия от директните вазодилататори най-вероятно се дължи на индуцираното от тези медикаменти рефлекторно повишено освобождаване на норадреналин и ангиотензин II. Тези субстанции стимулират развитието на левокамерната хипертрофия.
Библиография
1. Myerburg RJ, Castellanos A. Cardiac arrest and sudden cardiac death. In: Zipes DP, Libby P, Bonow RO, Braunwald E, ed. Braunwald’s Heart Disease: A Textbook of Cardiovascular Medicine. 7th edn. Elsevier Saunders Company, Philadelphia, PA, 2004: 865-908.
2. Myerburg RJ, Wellens JJ. Epidemiology of cardiac arrest. In: Priori SG, Zipes DP. Sudden Cardiac Death. A handbook for clinical practice, Blackwell Publishing, 2006: 3-20.
3. Bunch TJ, White RD, Gersh BJ, et al. Long-term outcomes of out-of-hospital cardiac arrest after successful early defibrillation. N Engl J Med 2003; 348: 2626-2633.
4. Loire R, Tabib A. Unexpected sudden cardiac death: result of 1000 autopsies. Arch Mal Coeur 1996; 89: 13-18.
5. Messika-Zeitoun D, Gersh BJ, Fondard O, et al. Sudden cardiac death and vascular heart diseases. In: Priori SG, Zipes DP. Sudden Cardiac Death. A handbook for clinical practice, Blackwell Publishing, 2006: 147-161.
6. Soler-Soler J, Galve E. Worldwide perspective of valve disease. Heart 2000; 83: 721–725.
7. Iung B, Baron G, Butchart EG, et al. A prospective survey of patients with valvular heart disease in Europe: the Euro Heart Survey on valvular heart disease. Eur Heart J 2003; 24: 1231–1243.
8. Salerno-Uriarte JA, Fantoni C, Marazzi R. What is sudden death? A correct identification. In: Capucci A. Sudden Cardiac Death, Informa Healthcare, 2007: 3-14.
9. Chizner MA, Pearle DL, deLeon AC Jr. The natural history of aortic stenosis in adults. Am Heart J 1980; 99: 419-424.
10. Bonow R, Carabello B, DeLeon A, et al. ACC/AHA guidelines for management of patients with valvular heart disease. Circulation 1998; 98: 1949-1984.
11. Iung B, Gohlke-Barwolf C, Tornos P, et al. Recommendations on the management of the asymptomatic patient with valvular heart disease. Eur Heart J 2002; 23: 1252-1266.
12. Otto CM, Burwash IG, Legget ME, et al. Prospective study of asymptomatic valvular aortic stenosis. Clinical, echocardiographic, and exercise predictors of outcome. Circulation 1997; 95: 2262-2270.
13. Rosenhek R, Binder T, Porenta G. et al. Predictors of outcome in severe, asymptomatic aortic stenosis. N Engl J Med 2000; 343: 611-617.
14. Amato MC, Moffa PJ, Werner KE, et al. Treatment decision in asymptomatic aortic valve stenosis: role of exercise testing. Heart 2001; 86: 381-386.
15. Das P, Rimington H, Smeeton N, et al. Determinants of symptoms and exercise capacity in aortic stenosis: a comparison of resting haemodynamics and valve compliance of aortic stenosis in the community. J Am Coll Cardiol 2002; 40: 1723-1730.
16. Rosenhek R, Klaar U, Schemper M, et al. Mild and moderate aortic stenosis. Natural history and risk stratification by echocardiography. Eur Heart J 2004; 25: 199-205.
17. Messika-Zeitoun D, Aubry MC, Detaint D, et al. Evaluation and clinical implications of aortic valve calcification by electron beam computed tomography. Circulation 2004; 110: 356-362.
18. Otto CM, Lind BK, Kitzman DW, et al. Association of aortic valve stenosis with cardiovascular mortality and morbidity in the elderly. N Engl J Med 1999; 341: 142-147.
19. Connolly HM, Oh JK, Orszulak TA, et al, Circulation 1997; 95: 2395-2400
20. Vahanian A, Baumgartner H, Bax J, et al. Guidelines on the management of valvular heart disease. The task force on the management of valvular heart disease of the European Society of Cardiology. Eur Heart J 2007; 28: 230-268.
21. Durjardin KS, Enriquez-Sarano M, Schaff HV, et al. Mortality and morbidity of aortic regurgitation in clinical practice. A long-term follow-up study. Circulation 1999; 99: 1851-1857.
22. Klodas E, Enriquez-Sarano M, Tajik AJ, et al., Optimizing timing of surgical correction in patients with severe aortic regurgitation: role of symptoms. J Am Coll Cardiol 1997; 30: 746-752.
23. Borer JS, Hochreiter C, Herrold EM, et al. Prediction of indications for valve replacement among asymptomatic or minimally symptomatic patients with chronic aortic regurgitation and normal left ventricular performance. Circulation 1998; 97: 525-534.
24. Bonow RO, Lakatos E, Maron BJ, et al. Serial long-term assessment of the natural history of asymptomatic patients with chronic aortic regurgitation and normal left ventricular systolic function. Circulation 1991; 84: 1625-1635.
25. Ling H, Enriquez-Sarano M, Seward J, et al. Clinical outcome of mitral regurgitation due to flail leaflet. N Eng J Med 1996; 335: 1417-1423.
26. Tribouilloy C, Enriquez-Sarano M, Schaff H, et al. Impact of preoperative symptoms on survival after surgical correction of organic mitral regurgitation: rationale for optimizing surgical indications. Circulation 1999; 99: 400-405.
27. Grigioni F, Enriquez-Sarano M, Ling LH, et al. Sudden death in mitral regurgitation due to flail leaflet. J Am Coll Cardiol 1999; 34: 2078-2085.
28. Freed LA, Levy D, Levine RA, et al. Prevalence and clinical outcome of mitral-valve prolapse. N Engl J Med 1999; 341: 1-7.
29. Flack JM, Kvasnicka JH, Gardin JM, et al. Anthropometric and physiologic correlates of mitral valve prolapse in a biethnic cohort of young adults: the CARDIA study. Am Heart J 1999; 138: 486-492.
30. Zuppiroli A, Rinaldi M, Kramer-Fox R, et al. Natural history of mitral valve prolapse. Am J Cardiol 1995; 75: 1028-1032.
31. Ling LH, Enriquez-Sarano M, Seward JB, et al. Early surgery in patients with mitral regurgitation due to flail leaflets: a long-term outcome study. Circulation 1997; 96: 1819-1825.
32. Kligfield P, Levy D, Devereux RB, et al. Arrhythmias and sudden death in mitral valve prolapse. Am Heart J 1987; 113: 1298-1307.
33. Haider AW, Larson MG, Guerot C. Increased left ventricular mass and hypertrophy are associated with increased risk for sudden death. J Am Coll Cardiol 1998; 32: 1454-1459.
34. Levy D, Garrison RJ, Savage DD, et al. Prognostic implications of echocardiographically determined left ventricular mass in the Framingham Heart Study N Engl J Med 1990; 322: 1561-1566.
35. Haider AW, Larson MG, Benjamin EJ, et al. Increased left ventricular mass and hypertrophy are associated with increased risk for sudden death. J Am Coll Cardiol 1998; 32: 1454-1459.
36. Franz IW, Tӧnnesmann U, Müller JF. Time course of complete normalization of left ventricular hypertrophy during long-term antihypertensive therapy with angiotensin converting enzyme inhibitors. Am J Hypertens 1998; 11: 631-639.






