Пациент на 37 години е с прогресивно влошаваща се болка в долната част на гърба. Той си спомня, че дори в тинейдърска възраст е имал спорадични болки в гърба. Липсвала е травма, разпознаваем фактор или събитие, които да бъдат асоциирани с болката. За първи път е потърсил лечение за болката си в гърба на 25 години. По това време е започнал лечение с ибупрофен 400 mg на всеки 6 часа, който е облекчил значително симптомите. Но 5 години по-късно е развил нетърпими гастроинтестинални (GI) странични ефекти. Лечението е заменено с напроксен 220 mg два пъти дневно. Чувствал е облекчение за известно време, но в момента съобщава, че болката не е адекватно контролирана. Съобщава още, че болката в гърба е по-силна сутрин и се успокоява до известна степен след като стане от сън и се раздвижи. Болката често нарушава нощния му сън за около 3-4 часа. Прилагал е хиропрактично лечение, както и физиотерапия за болката в гърба, но нито едно от тях не е облекчило симптомите (Табл. 1 и 2). (Най-честата терапевтична процедура, извършена от хиропрактика е известна като „гръбначна манипулация“, наричана също „хиропрактична корекция.“- основната мануална техника на хиропрактиката. Тя се състои в умерен натиск върху определена точка, който отговаря на две задължителни условия – голяма скорост и слаба амплитуда на движението)
Табл. 1. Анамнеза и находки от физикалния преглед
|
Анамнеза |
Находки |
|
Медицинска |
|
|
Лечения |
Напроксен 220 mg 2 пъти дневно |
|
Алергиии |
NKDA |
|
Операции |
Няма |
|
Фамилна |
Майка на 65 г. |
|
Социален статус |
Неженен |
|
Физикален преглед |
Находки |
|
Жизнени показатели |
BP 128/84 mm Hg; пулс 75/min, нормален; вдишвания 12/min; температура 37ºС; O2 сатурация 95%, BMI 28 kg/m2 |
|
Общи |
В момента няма остър дистрес. (Настъпването на трайни увреждания в организма – функционални или органични от продължителен увреждащ стрес се определя като дистрес.) |
|
Кожа |
Нормална, без доказателства за псориазис |
|
HEENT |
Нормални |
Бял дроб,аускултация |
Без патологични шумове двустранно и странично |
|
Сърце |
Нормални сърдечни тонове, без шум |
|
Корем |
Твърд, липсва органомегалия |
|
Опорно-двигателен апарат |
|
|
Неврологични |
Без фокален дефицит |
BMI = индекс на телесна маса; BP = кръвно налягане; HEENT = глава, очи, уши, врат, гърло; NKDA= неизвестни алергии към лекарства
Табл 2. Лабораторни тестове
|
CBC |
Резултати |
|
WBC |
7.8 K/cu mm |
|
HGB |
14.0 g/dL |
|
HCT |
43% |
|
Тромбоцитно броене |
306 K/cu mm |
|
Метаболитен панел |
Резултати |
|
Натрий |
137 mEq/L |
|
Калий |
5.1 mEq/L |
|
Хлориди |
101 mEq/L |
|
CO2 |
25 mEq/L |
|
Креатинин |
0.9 mg/dL |
|
BUN |
17 mg/dL |
|
eGFR |
100 mL/min/1.73 m2 |
|
Глюкоза |
98 mg/dL |
|
ESR |
21 mm/h |
|
CRP |
0.6 mg/dl |
BUN = урея; CBC = пълна кръвна картина; CRP = C-рективен протеин; eGFR = прогнозна скорост на гломерулна филтрация; ESR = скорост на утаяване на еритроцити; HCT = хематокрит; HGB = хемоглобин; WBC = бели кръвни клетки
Въпрос:
Каква е клиничната Ви диагноза въз основа на медицинската анамнеза и резултатите от физикалния преглед?
- Реактивен артрит
- Анкилозиращ спондилит (AS)
- Аксиален спондилоартрит (axSpA)
Верен отговор: Аксиален спондилоартрит
В този клиничен случай няколко са факторите, които навеждат на мисълта, че става въпрос за axSpA: прогресивно влошаваща се болка в гърба, с начало в тинейджърска възраст, подобрение при физическа активност и влошаване при покой, смущения в съня и добър отговор на лечение с нестероидни противовъзпалителни средства (NSAIDs). Освен това от анамнезата увеит, плантарен фасциит и тендинит на Ахилесовото сухожилие са силни показатели за имунно-медиирано възпалително ревматично заболяване.
Дискусия
Спондилоартритът (SpA) описва сбор от хронични възпалителни ревматични заболявания с припокриващи се характеристики, вкл. засягане на периферна и аксиална става като сакролит, ентензит, периферен възпалителен артрит, извънставни прояви, позитивен човешки левкоцитен антиген (HLA)-B27 и фамилни фактори. Характерно за аксиалния спондилоартрит (axSpA) е засягането на сакроилиачните стави и гръбначния мозък. Често диагнозата axSpA се поставя късно, понякога след 8 и повече години. Главната причина за късното поставяне на диагнозата е, че сакролитът, който се счита отличителен белег на анкилозиращия спондилит (AS), не е клинично откриваем и може да не бъде видян при рентгенова снимка в ранните стадии на заболяването.
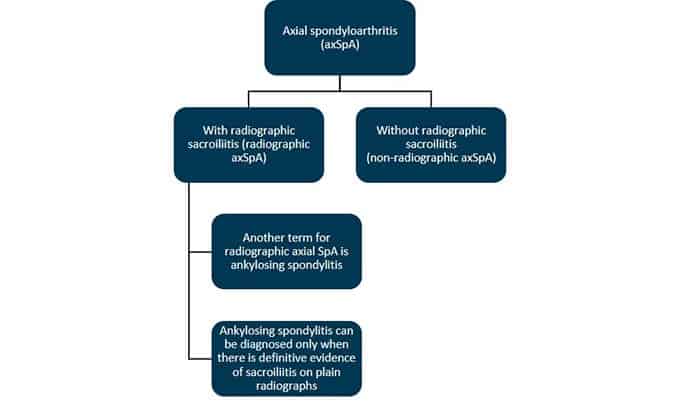
Съществуват два основни вида SpA – аксиален и периферен, в зависимост от основните проявяващи се симптоми. Обаче, двата вида могат да се припокрият и единият да прогерсира спрямо другия. Аксиалният SpA засяга главно гръбнака и сакроиличаните стави. Периферният SpA засяга предимно периферните стави. За целите на класификацията axSpA се разделя впоследствие на axSpA с рентгенографски данни и axSpA без рентгенографски данни (Фиг.1)
Фиг. 1. Спектър на axSpA
Превод на схемата:
Аксиален спондилоартрит
(axSpA)
Със сакролит с рентгенографски данни Без сакролит с рентгенографски данни
(axSpA с рентгенографски данни) (axSpA без рентгенографски данни)
Друг термин за аксиалния SpA с
рентгенографски данни е анкилозиращ спондилит
Анкилозиращият спондилит може да се
диагностицира само, когато има категорично
доказателство за сакролит от обикновена
рентгенова снимка
Еволюиращото разбиране за понятието axSpA е довело до различаване между axSpA без рентгенографски данни axSpA (nr-axSpA) и axSpA с рентгенографски данни. Тези 2 термина се различават по степента на сакроилит, оценен от конвенционална рентгенография. AxSpA с рентгенографски данни, или AS, може да се диагностицира единствено при наличие на опеределено доказателство за сакроилит при рентгенови снимки за сакроилиак.
Важно е да се припомни, че в клиничната практика рентгеновата снимка за сакроилит е късна находка в хода на заболяването на много пациенти. Пациентите могат да бъдат диагностицирани въз основа на обикновен клиничен модел, дори и при наличие на нормални рентгенови снимки. Водещият симпмтом при axSpA е хронична болка в гърба, „възпалителна“ по своята същност, която се подобрява при физическа активност и не се успокоява при покой. В допълнение, други опорно-двигателни прояви на axSpA включват артрит, ентезит и дактилит. Някои типични извънставни прояви при пациенти трябва да наведат на мисълта за клинично подозрение за axSpA. Те могат да включват остър преден увеит (AAU), псориазис и възпалително чревно заболяване (IBD).
В конкретния случай пациентът е имал 3 прояви на увеит, което е често срещано при пациенти с axSpA. В крос-секционно проучване при пациенти с AS, 39% са били с анамнеза AAU. В системен обзор и мета-анализ общото разпространение на AAU е било 25.8%. Проучване на неселектирани пациенти с увеит е установило минимално разпространение на axSpA от 20.2%. От тези пациенти, 22.9% не са били с предишна диагноза axSpA.
Решаващите елементи за бързата и правилна диагноза включват подорбна анамнеза на представеното оплакване и предишна медицинска анамнеза. Хронологията на болката и описанието на отежняващите фактори предоставят доказателства за диагнозата. Пациенти с axSpA обикновено описват изявена скованост и намаление на болката при физическа активност или упражнения.
При конкретния случай рентгеновата снимка на сакроилиачната става не показва доказателство за сакроилит. Тестът за HLA-B27 е положителен.
Въпрос:
Кой от следните изброени способи би бил най-ефикасен за потвърждение на диагнозата axSpA без рентгенографски данни (nr-axSpA)?
- Ядрено-магнитен резонанс (MRI) на лумбалните прешлени
- Рентгенова снимка на торакалната част на гръбнака за наличие на синдесмофит
- MRI на сакроилиачните стави с гадолиний
- MRI на сакроилиачните стави без гадолиний
Верен отговор: MRI на сакроилиачните стави без гадолиний
MRI на сакроилиачните стави потвърждава диагнозата, но гадолиний не е необходим. Важно е да се направи T1-претеглено изображение и претеглено изображение на Т2 мастно потискане (STIR секвенция). Трябва да се избегнат разходите и страничните ефекти, свързани с гадолиний, тъй като по-ясното изображение, което се получава с гадолиний не помага за диагностициране в областта на T1 и STIR изображенията.
Дискусия
MRI може да покаже признаци на възпаление, много по-рано отколкото рентгеновите снимки могат да покажат структурно увреждане. MRI позволява ранно откриване на възпаление на сакроилиачната става при пациенти с axSpA. При по-доброто изображение с гадолиний може да се открият участъци с повишена васкуларизация, спомагащи за откриване на синовит и ентезит; но не е необходимо да се добавя диагностичен капацитет на MRI в областта на STIR и T1 секвенции при диагностициране на ранен axSpA. През възпалителната фаза STIR изображение обикновено показва хиперинтензитет на костния мозък (едем на костния мозък) двустранно на сакроилиачните стави. За да се спести време, неудобство за пациета, разходи и риск, не е необходимо приложение на гадолиний.
На пациента е направен MRI на сакроилиачни стави. T1-претегленото изображение показва доказателство за ерозия и склероза, а STIR изображението показва доказателство за едем на костния мозък в базалния ъгъл на илио-сакралната става. Диагнозата nr-axSpA се потвърждава въз основа на тези находки от образната диагностика.
Въпрос:
Коя от следващите стъпки е най-добра за пациента според насоките на Американския колеж по ревматология (ACR)/Американската асоциация по спондилит (SAA)/(SPARTAN)?
- Повшение на дозата NSAID и добавяне на физиотерапия
- Започване с инхибитор на тумор-некрозиращия фактор (TNF), тъй като при него заболяването е в активна форма и е рефракторно на NSAID
- Започване на лечение със сулфазалазин
- Започване с преднизон 1 mg/kg/d за 10 дни, последван от затихваща терапия в течение на1 месец
Верен отговор: Започване с инхибитор на тумор-некрозиращия фактор (TNF), тъй като при него заболяването е в активна форма и е рефракторно на NSAID
Първият избор на лечение на axSpA без рентгенографски данни (nr-axSpA) обикновено включва NSAIDs и физиотерапия. Но понастоящем заболяването на пациента е в активна форма и е рефракторно на NSAIDs. В такива случаи ACR/SAA/SPARTAN съветва употреба на TNF инхибитор. Въз основа на много малките до умерени доказателства за наличие на слаби клинични ефекти или липса на такива, ACR/SAA/SPARTAN препоръчва в замяна употребата на бавнодействащи антиревматични средства (SAARDs) при повечето пациенти, чийто AS остава в активна форма, независимо от употребата на NSAID.
Дискусия
Нестероидните противовъзпалителни средства (NSAIDs) се препоръчват като първи избор на лечение на nr-axSpA. Въпреки че са ефективни при намаление на възпалението, болката и сковаността, трябва да се знае, че те могат да предизвикат кървене от ГИТ и кардиотоксичност. За заболявания, рефракторни на NSAIDs и за пациенти, които не могат да приемат NSAIDs, насоките препоръчват употреба на биологично лекарство като TNF инхибитор или инхибитор на интерлевкин (IL) 17.
FDA не е одобрила лечения за nr-axSpA; обаче, насоките за лечение на (ACR), а така също и на Европейската лига срещу ревматизма (EULAR) препоръчват употребата на някои лекарства, показани за AS при пациенти с nr-axSpA. 5 TNF инхибиторите, които са демонстрирали ефикасност при nr-AxSpA и са одобрени от FDA за лечение на AS са:
- Адалимумаб
- Цертолизумаб пегол
- Етанерцепт
- Голимумаб
- Инфликсимаб
Секукинумаб е първият IL-17 инхибитор, одобрен от FDA за лечение на AS. В ход са проучвания на IL-17 инхибитори при пациенти със заболяване без рентгенографски данни. Трябва да се подхожда с внимание при обмисляне на IL-17 инхибитори при пациенти с axSpA, с активна форма на заболяване на дебелото черво или болест на Крон. Трябва също да се отбележи, че и TNF инхибиторите и IL-17 инхибиторите могат повторно да активират латентна туберкулоза и да повишат риска от инфекция.
ACR/SAA/SPARTAN силно препоръчва в замяна лечение със системни глюкокортикостероиди при активни форми на АS и nr-axSpA. Има ограничени проучвания за лечение на активна форма на AS със системни глюкокортикостероиди, които са показали скромни подобрения; обаче, броят на контролите при рандомизираните контролни проучвания (RCT) е бил малък и е счетено, че доказателствената стойност на проучванията е ниска, поради риск от отклонение и неточност при оценка на ефекта.
Лечението на пациенти с axSpA трябва да бъде индивидуализирано според състоянието на пациента и остротата на заболяването, а така също и според характеристиките на пациента като съпътстващи заболявания и физиологични фактори. AxSpA се свързва с няколко съпътстващи заболявания, които допринасят значително за заболеваемостта и смъртността, а така също и за сложността на лечението. Тези съпътстващи заболявания включват хипертония, хиперлипидемия, захарен диабет, пептични язви, главоболие, увеит, рак, IBD, остеопороза, псориазис и други сърдечно-съдови, белодробни, бъбречни и неврологични усложнения. Следователно, важно е да се вземат под внимание всички съпътстващи заболявания при изграждане на планове за лечение и пациентите да се насочат своевременно към специалист.
В допълнение към фармакологичната терапия, пациентите трябва да бъдат съветвани да правят редовно физически упражнения. Препоръчват се упражнения в домашни условия, тъй като те са с доказана полза при пациенти с axSpA. Физиотерапията е още по-полезна и за всеки пациент трябва да се обмисли физиотерапия, като решението се взима индивидуално.
Пациентите трябва да бъдат обучени на всичките аспекти при лечение на тяхното заболяване и да бъдат насърчавани да участват при взимане на решение, относно лечението им. Мониторирането на заболяването на пациенти с axSpA в клинични условия би могло да включва оценка на активността на заболяването, резултати, съобщени от пациента, клинични находки, лабораторни тестове и образна диагностика. Решението за видовете и честотата на мониториране трябва да бъде взето индивидуално, взависимост от симптомите, остротата и лечебния режим. За определяне нивото на активност на заболяването може да се използва индексът Bath Ankylosing Spondylitis Disease Activity Index (BASDAI) или Ankylosing Spondylitis Disease Activity Score (ASDAS). (Фиг. 2 и 3) В миналото в клиничната практика активната форма на заболяване е била дефинирана като BASDAI скор ≥4, но тя може също да се дефинира като ASDAS ≥2.1.
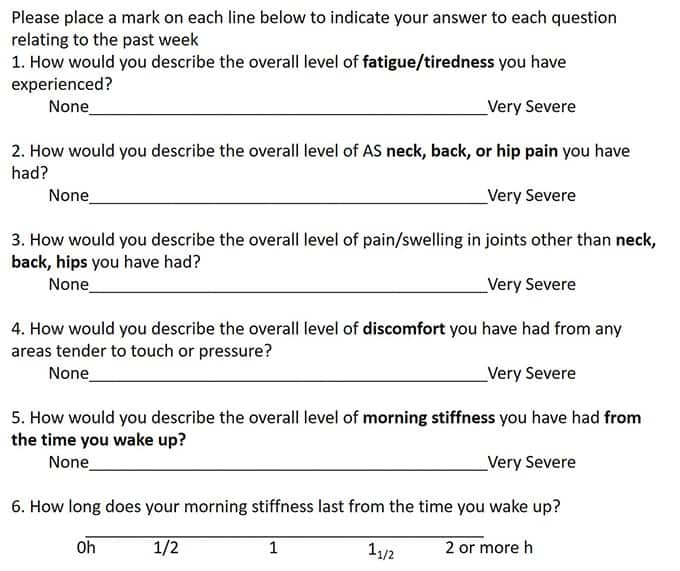
Фиг. 2. BASDAI скор
Превод на фиг.2
Моля, отбележете на всеки ред по-долу Вашия отговор на всеки въпрос, отнасящ се до изминалата седмица
1.Как бихте описали общото ниво на изтощение/умора, което сте изпитвали?
Липсва ______________________________________________________________Много тежко
2.Как бихте описали общото ниво на болка от AS във врата, гърба или кръста, която сме имали?
Липсва ______________________________________________________________Много тежко
3.Как бихте описали общото ниво на болка/подуване в ставите, различна от тази във врата, гърба или кръста, която сме имали?
Липсва ______________________________________________________________Много тежко
4.Как бихте описали общото ниво на дискомфорт, което сте имали, предизвикан от участъци, чувствителни при допир или натиск?
Липсва ______________________________________________________________Много тежко
5. Как бихте описали общото ниво на сутрешна скованост, която сте имали от времето на събуждане?
Липсва ______________________________________________________________Много тежко
6. Колко трае сутрешната Ви скованост от времето на събуждане?
______________________________________________________________
0 h ½ h 1 h 1½ h 2 или повече h
Фиг. 3a. ASDAS параметри и изчисления
Превод на фиг. 3А
Параметри
Обща болка в гърба (0-10)
Глобална оценка на пациента (0-10)
Периферна болка/подуване (0-10)
Продължителност на сутрешна скованост (0-10)
CRP в mg/L (или ESR mm/hr) (най-ниската стойност за CRP може да бъде 2 mg/L)
Изчисления
ASDAS-CRP: 0.121 х общата болка + 0.110 х глобалната оценка на пациента + 0.073 х периферната болка/подуване + 0.578 x продължителността на сутрешната скованост + 0.579 xln (CRP + 1)
ASDAS-ESR: 0.113 х глобалната оценка на пациента + 0.293 xv ESR +0.086 x периферната болка/подуване + 0.069 x продължителността на сутрешната скованост + 0.079 x общата болка
Отговорете на всеки въпрос, като отбележите от 0 (липсва) до 10 (много тежко)
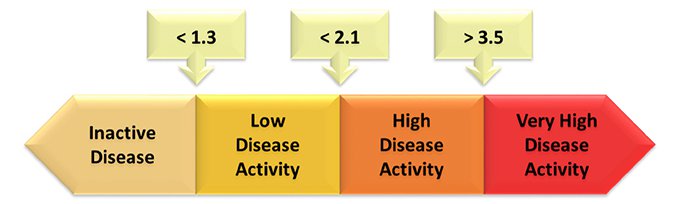
Фиг. 3b. 2018 Актуализиране на номенклатурата за стадиите на ASDAS
Превод на фиг. 3b
Неактивна форма на заболяването
Ниска активност на заболяването
Висока активност на заболяването
Много висока активност на заболяването
Предполага се, че активността на заболяването се измерва по-добре чрез ASDAS, отколкото чрез BASDAI. В подкрепа на това заключение е факта, че BASDAI е мярка, изцяло въз основа на резултата, който пациента съобщава, докато ASDAS се основава и върху съобщенията на пациентите, и върху C-реактивния протеин. В допълнение, ASDAS изключване на активност на заболяването и критерии на отговор са били базирани върху обстоен процес на валидиране, докато BASDAI критерии за изключване са били избрани произволно. Освен това, докато постоянно повишаващият се ASDAS се свързва с формиране на синдесмофити, то BASDAI трябва да бъде комбиниран с CRP измерване, за да има същата стойност. Въпреки че често има съгласуваност между BASDAI скор ≥4 и ASDAS ≥2.1, в несъгласувани случаи повишеният ASDAS предсказва по-добър отговор, отколкто повишеният BASDAI.
Скорът BASDAI на пациента е 5, а ASDAS – 2.6. Той започва лечение с инфликсимаб 5 mg/kg в началото на лечението, в седмица 2, в седмица 6, а след това на всеки 6 седмици и се чувства добре. При последващи проследявания през годината неговият BASDAI скор се подобрява до 1.9. Но година по-късно започва да изпитва инфузионни реакции. По време на визитата си той е отново симптоматичен и отбелязва, че болките в гърба са се усилили отново. По време на визитата BASDAI скорът му е 6.4.
Въпрос:
Какви приспособявания трябва да се направят на лечението на пациента?
- Предписване на наркотични аналгетици и продължаване лечението с инфликсимаб в същата доза
- Повишение дозата инфликсимаб до 7.5 mg всеки 4 седмици
- Превключване на иксекизумаб
- Превключване на адалимумаб
Верен отговор: Превключване на адалимумаб
Пациентът изпитва късна инфузионна реакция, а също така намалена ефикасност от лечението с инфликсимаб. Според настоящите препоръки след „повторен“ неуспех на първоначален TNF инхибитор, пациентът трябва да бъде превключен на втори TNF инхибитор. По това време иксекизумаб все още не е бил одобрен за лечение на axSpA, така че той не е могъл да бъде най-добрият избор за него, въз основа на текущото доказателство. Трябва да се избягват възможно най-дълго наркотичните аналгетици при лечение на хронични възпалителни заболявания като активната форма на axSpA, поради свойството им да предизвикват привикване.
Инфузионни реакции от инфликсимаб могат да се получат по всяко време в хода на лечението, дори при пациенти, които са понасяли лечението преди това. Обаче, в проспективен анализ на пациенти, включени в общински регистър, инфузионните реакции от инфликсимаб са били нечести и обикновено са били класифицирани като леки до умерени. В 7-годишен анализ на 1632 пациенти, 63.1% са били лекувани за ревматологични състояния като ревматоиден артрит, AS, или псориатичен артрит. Най-честите инфузионни реакции са били сърбеж (19.9%), зачервяване (9.9%) и диспнея (6.2%). Около 2/3 от инфузионните реакции са били наблюдавани през първата година от лечението.
Скорошни анализи препоръчват, че превключването на TNF инхибитори може да е ползотворно при редица пациенти с axSpA, при които има вторична загуба на отговор на първоначална терапия с TNF инхибитори. В Европа TNF инхибиторите са показани за axSpA, вкл. за тези с рентгенографски данни, доколкото съществува доказателство за активно възпаление. Понастоящем в САЩ индикацията се ограничава до AS.
Понастоящем адалимумаб е показан за AS и се препоръчва за nr-axSpA, въз основа на данни от клинични проучвания.
В рандомизирано, контролирано проучване ABILITY-1 адалимумаб е имал положителен профил полза-риск при пациенти с активен nr-axSpA. Били са демострирани по-големи подобрения в активността на заболяването, физическата функция и здраве, свързано с качеството на живот, а така също и понижение на възпалението в сакроиличаната става и гръбнака, въз основа на находки от MRI след 12-седмична терапия с адалимумал в сравнение с плацебо (Табл. 3). В отворено продължение на ABILITY-1 пациентите с nr-axSpA са имали продължителни клинични и функционални подобрения в продължение на 3 години, а така също и потискане на MRI аксиалното възпаление, което е било по-голямо при пациенти, постигнали клинична ремисия. Профилът на безопасност е бил последователен с това, което е било наблюдавано при адалимумаб при AS и други заболявания.
Понастоящем има няколко други TNF инхибитори, които са одобрени в индикация nr-axSpA в Европа и в други страни, но не и в САЩ. Те включват сертолизумаб, етанерцепт и голимумаб. Данни от няколко неотдавнашни клинични проучвания са демонстрирали добър профил на ефикасност и безопасност за тези агенти за nr-axSpA (Табл. 3).
Табл. 3. Фаза 3 проучвания на TNF инхибитори, одобрени понастоящем за AS и в процес на проучване за лечение на nr-AxSpA
|
Име на проучването |
Проучвано лекарство |
Продължи-телност на проучваето |
Популация пациенти |
Брой пациенти |
Резултати |
|
ABILITY-1 |
Адалимумаб 40 mg на всеки 2 седмици |
12 седмици |
Активен nr-axSpA Общ скор на болката в гърба ≥4 на 0-10 cm VAS и BASDAI score ≥4 Неадекватен отговор или непоносимост към ≥1 NSAID |
Адалимумаб: n=91 Плацебо: n=94 |
ASAS40: 36% с/у 15% |
|
RAPID-axSpA |
Сертолизумаб пегол SC 200 mg на всеки 2 седмици Certolizumab pegol SC 400 mg на всеки 4 седмици |
24 седмици |
Активен axSpA (BASDAI ≥4 и общ скор на болка в гърба ≥4 на VAS 0-10 cm, повишен CRP и/или сакроилит при MRI) Неадекватен отговор или непоносимост към ≥1 NSAID в продължение на ≥30 дни продължителна терапия (най-високата поносима доза) или ≥2 седмици всяко за ≥2 NSAIDs |
Сертолизумаб пегол 200 mg: n=111 (обща axSpA популация) Сертолизумаб пегол 400 mg: n=107 (обща axSpA популация) Плацебо: n=107 Nr-axSpA: 147 пациенти от 325 |
ASAS20 в седмица 12 за сертолизумаб пегол 200 mg с/у плацебо: 58.7% с/у 40.0% ASAS20 в седмица 12 за сертолизумаб пегол 400 mg с/у плацебо: 62.7% с/у 40.0% |
|
EMBARK |
Етанерцепт SC 50 mg веднъж седмично+ придружаваща терапия NSAID |
12 седмици |
Активен nr-axSpA (BASDAI ≥4) с неадекватен отговор към ≥2 NSAIDs, приети поотделно за обща комбинирана продължителност >4 weeks Продължителност на симптомите >3 месеца и <5 години Възраст: 18-49 години |
Етанерцепт: n=106 Плацебо: n=109 |
ASAS40: 32% с/у 16% |
|
GO-AHEAD |
Голимумаб SC 50 mg на всеки 4 седмици |
16 седмици двойно сляпо |
Активен nr-axSpA (BASDAI ≥4 и обща болка в гърба ≥4 при VAS 0-10 cm) Продължителност на симптомите ≤5 години Възраст: 18-45 години Неадекватен отговор или непоносимост към ≥1 NSAID |
Голимумаб: n=97 Плацебо: n=100 |
ASAS20 в седмица 16: 71% в/у 40% |
ASAS20 = Международно дружество за оценка на спондилоартрита 20%; ASAS40 = Международно дружество за оценка на спондилоартрита 40%; SC = подкожно; VAS = визуална аналогова скала.
Иксекизумаб е моноклонално антитяло, което се свързва избирателно с IL-17A цитокин и инхибира неговото взаимодействие с IL-17 рецептора. В проучване фаза 3 (представено в абстрактна форма), оценяващо безопасността и ефикасността на иксекизумаб при пациенти с активен AS, които никога не са получавали bDMARD, първоначалните крайни цели са постигнати в седмица 16 в групата с иксекизумаб (част от 52-седмично проучване). Сигнификантно повече пациенти са постигнали ASAS40 в седмица 16 с иксекизумаб q2w (52%) и иксекизумаб q4w (48%) с/у плацебо (18%, P<.001). И при двете дози иксекизумаб също е имало по-голямо подобрение на активността на заболяването, функционалната недостатъчност и спиналното и SIJ възпаление. Честотата на нежеланите събития, произтичащи от лечението е била подобна при иксекизумаб в сравнение с плацебо.
Тофацитиниб е орален инхибитор на Янус киназа (JAK), инхибиращ клетъчно сигнализиране през JAK3 и JAK1, и в по-ниска степен JAK2. В 16-седмично проучване с вариращи дози във фаза 2, тофацитиниб 5 или 10 mg два пъти дневно е демонстрирал по-вискока клинична ефикасност от плацебо при понижение на признаците, симптомите и целевите крайни точки на активния AS при възрастни. Според post hoc анализа на това проучване, приблизително 1/3 от пациентите, лекувани с тофацитиниб, са имали понижение на клинично изразеното спинално MRI възпаление в седмица 12. Почти 3 пъти повече пациенти, лекувани с тофацитиниб, са постигнали минимално важна промяна в MRI възпалението в сравнение с плацебо групата.
Заключение
Пациентът започва лечение с адалимумеб 40 mg на всеки 2 седмици. На проследяващата визита след 3 месеца неговият BASDAI скор е 2 и той съобщава, че се чувства доста по-добре.