Брой 6/2012
К. Семкова, Ж. Казанджиева
Катедра по дерматология и венерология,
Медицински университет – София
Хемангиомите са най-често срещаните доброкачествени съдови тумори при деца на възраст до 1 година, като засягат приблизително 4-5 до 10% от родените в нормална гестационна възраст (1, 2) и до 30% от недоносените кърмачета (3). Специфична характеристика на хемангиомите е типичната еволюция в три фази – бърза пролиферативна фаза, фаза на стабилизация и стациониране и фаза на бавна спонтанна регресия. Прекурсорна лезия под формата на хипо- или хиперпигментна макула може да се наблюдава още при раждането при около 50% от засегнатите деца, а при останалите хемангиомите се появяват в първите дни или седмици след раждането и до 9-ата година претърпяват обратно развитие при около 90%. Въпреки бенигнения характер и обратното развитие при 25-69% от пациентите на мястото на хемангиома остават телангиектазии, фиброзно-мастна тъкан, атрофично набръчкване на кожата или цикатрикси (4). Фактори за повишен риск от развитие на козметични усложнения са разположение в централната част на лицето, развитие на улцерации и нодуларна форма на хемангиома.
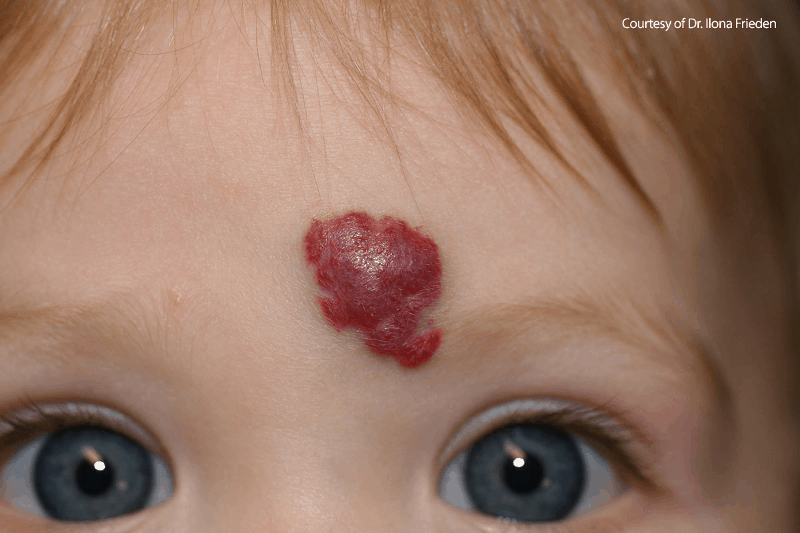
Клиничната картина на хемангиомите зависи от разположението и дълбочината им. Повърхностните хемангиоми са яркочервени, надигнати плаки или нодули, докато дълбоките хемангиоми са плътни образувания с неясни граници, синкав оттенък и непроменена надлежаща кожа. При смесените хемангиоми има наличие както на повърхностна, така и на дълбока компонента. Повърхностните хемангиоми са локализирани или сегментни. Сегментните обхващат една или повече анатомични области и са асоциирани с по-висок риск от животозастрашаващи усложнения и структурни аномалии. В някои случаи детските хемангиоми може да са част от симптомокомплекс на клинични синдроми, което усложнява диагностичното уточняване и налага комплексен терапевтичен подход. Такива синдроми са хемангиоматоза и синдромите PHACES и LUMBAR (5).
Етиопатогенезата на детските хемангиоми не е напълно изяснена и понастоящем съществуват различни хипотези – плацентарен произход; генетичен дефект или соматична мутация на ендотелните клетки; влияние на външни фактори, които създават благоприятна среда за клетъчна пролиферация.
Показания за лечение
Повечето малки хемангиоми претърпяват пълно обратно развитие и стандартното поведение при тях е „активна ненамеса”, която се изразява в активно проследяване и терапевтична намеса само при развитие на усложнения.
Конвенционалните показания за активна намеса може да се разделят на три основни групи: 1. Профилактика или лечение на функционално нарушение или болка (поява на улцерация, периорбитално разположение със засягане на зрението, лумбосакрални хемангиоми, хемангиоми в областта на гърлото, ограничаващи движенията сегментни хемангиоми на крайниците); 2. Профилактика или лечение на цикатрикси и/или деформации (екзофитни хемангиоми, хемангиоми с дълбока дермална компонента, акрални хемангиоми на главата, хемангиоми на върха на носа, сегментни хемангиоми на лицето като част от PHACES и/или при риск от нарушаване на анатомията на лицето и функционално нарушение); 3. Избягване на животозастрашаващи усложнения (хемангиоми на дихателните пътища, симптоматични чернодробни хемангиоми) (6). Лечението трябва да започне възможно най-рано през пролиферативната фаза, за да се избегнат усложненията, които може да възникнат при нарастване на хемангиома. Такива усложнения са улцерации, кървене, инфекция и сърдечна недостатъчност (7).
Все повече клиницисти обаче се насочват към терапевтично повлияване дори и без стриктни индикации, за да се предотвратят потенциалните усложнения и козметични дефекти. Много родители предпочитат активната намеса пред изчакване на обратното развитие поради неблагоприятното психологическо и емоционално въздействие за семейството и детето, когато хемангиомите са разположени във видими области на тялото.
Конвенционални методи на лечение
Конвенционалните средства за лечение на хемангиомите при кърмачета и деца включват системно, интралезионално и локално приложение на кортикостероиди, както и лазерни и хирургични интервенции. При животозастрашаващи хемангиоми и противопоказания за приложение на стероиди или оперативно отстраняване може да се обмисли системно приложение на интерферон, винкристин или циклофосфамид, като се вземат под внимание техните сериозни странични ефекти. В миналото за първо средство на избор при необходимост от лечение на детските хемангиоми се приемаха системните стероиди. Те са показали добра ефективност и опитът с тях е дългогодишен, което позволява да се очакват и проследяват първите признаци и симптоми на очакваните странични ефекти.
Нови подходи на лечение
Системни бета-блокери
Пропранолол е неселективен β-адренергичен антагонист, който инхибира конкурентно β1- и β2-адренорецепторите, експресирани на повърхността на ендотелните клетки. Прилага се в кардиологията за лечение на артериална хипертония, сърдечни ритъмни нарушения, хипертрофична кардиомиопатия, тиреотоксикоза, мигрена и есенциален тремор.
Антипролиферативният ефект на пропранолол при детските хемангиоми е открит случайно през 2008 г. от Léauté-Labrèze и колектив (8). Те прилагат пропранолол за лечение на обструктивна хипертрофична кардиомиопатия, индуцирана от кортикостероидна терапия за назален хемангиом. Хемангиомът започва да променя цвета и консистенцията си още първия ден след започване на лечението и изчезва напълно за няколко месеца.
Съобщението на Léauté-Labrèze et al. промени напълно представата за терапията при хемангиомите в детска възраст и беше последвано от множество съобщения на единични или серии от случаи на успешно повлияване с пропранолол. Бърза регресия може да се постигне при сегменти и усложнени хемангиоми, хемангиоми на дихателните пътища, периорбитални хемангиоми, застращаващи зрението, орбитални хемангиоми, хемангиоми с бърза пролиферация, PHACES, чернодробни хемангиоми и хемангиоматоза. Хемангиоми във фаза на инволюция също се повлияват успешно от лечение с пропранолол, поради което бета-блокерите може да се наложат като средство на избор при пациенти, за които не е потърсена адекватна терапия в ранната фаза или ранните активни интервенции не са дали резултат (9).
Механизъм на действие
Механизмът на действие на пропранолол при детските хемангиоми не е напълно изяснен. Приема се, че ефективността му се дължи на три допълващи се фармакодинамични характеристики – вазоконстрикция, инхибиране на ангиогенезата и индукция на апоптозата (10). Клинично тези три механизма се транслират в бързо инициално изсветляване на повърхността на хемангиома, спиране на растежа и постепенна регресия.
Безопасност
Опитът от приложението на пропранолол при деца в кардиологичната практика е от повече от 40 години и профилът му на нежелани реакции в тази възрастова група е относително благоприятен без документирани случаи на фатален изход или развитие на сериозно заболяване в резултат на директна експозиция на бета-блокер (11). Повечето реакции са предсказуеми и са в резултат на блокиране на рецепторите. Най-често наблюдаваните нежелани лекарствени реакции при лечение на деца с пропранолол са хипотония, синусова брадикардия, хипогликемия и бронхоспазъм, които обикновено не са животозастрашаващи (12), но налагат сериозно мониториране на пациента преди и по време на терапията. Особено внимание е необходимо при децата с много големи хемангиоми, съдови малформации, PHACES, малформации на външните гениталии, липомиеломенингоцеле, везикоренална патология и LUMBAR синдром, при които пропранололът може да маскира ранните симптоми на развиваща се сърдечна недостатъчност или да влоши функционалния капацитет на сърцето (12).
Съобщавани са случаи на тежка хипогликемия и/или хипотермия при деца с хемангиоми на лечение с пропранолол (13, 14). Рискът е по-висок при деца, които приемат редуцирано количество храна, и при тях кръвната захар трябва да се проследява по-често или приемът да се преустанови до възстановяване на нормално хранене. За профилактиране на хипогликемията се препоръчва детето да се храни след приложение на всяка доза пропранолол.
Въпреки благоприятния профил на безопасност лечението с пропранолол трябва да се започне с повишено внимание и при стриктно проследяване от дерматолог или педиатър с опит в приложението му. Повечето автори прилагат своя терапевтична схема, тъй като няма фармакокинетични данни и проспективни контролирани изпитвания за оптимално дозиране в тази възрастова група пациенти. Продължителността на лечението зависи от терапевтичния ефект, но за да не се получи значим рецидив, бета-блокерът трябва да се прилага до приключване на пролиферативната фаза, която може да продължи до 8-12 месеца (15).
Забележителната ефективност и добрата поносимост на пропранолол го правят добър кандидат за средство на избор за лечение на хемангиоми в кърмаческа и детска възраст. Въпреки дългогодишната практика на лечение с кортикостероиди и доброто познаване на техните параметри при приложение при деца все повече специалисти предлагат пероралните бета-блокери като първа терапевтична линия (16, 17).
Локални бета-блокери
Timolol maleate (тимолол малеат) е неселективен бета-блокер, който се използва в офталмологията за лечение на глаукома с отворен ъгъл и на вторична глаукома под формата на разтвор и гел за локално приложение.
Ефективността на тимолол гел и разтвор в различни концентрации за лечение на хемангиоми при деца е показана при ограничен брой пациенти, без да са наблюдавани нежеланите реакции, характерни за системното приложение на пропранолол.
Системната бионаличност на тимолол, приложен като капки в очите, при здрави доброволци е около 50%. Нежеланите реакции, съобщавани при лечение на глаукома при деца включват сънливост, брадикардия, сърбеж в окото, дишане тип Cheyne-Stokes, епизоди на апнея и тежко влошаване на предшестваща астма (18).
Нашият опит за лечение на хемангиоми с локални бета-блокери показа изключително добри резултати при първата група от 20 деца на възраст от 3 месеца до 2 години. Ние смятаме, че локалните бета-блокери са добра алтернатива на системните бета-блокери за лечение на повърхностни хемангиоми със сходна ефикасност, но по-добра поносимост. Трябва обаче да не се пренебрегва рискът от развитие на потенциални нежелани реакции поради несъвършената бета-адренергична регулация и повишената трансдермална абсорбция при кърмачета. Локалните бета-блокери трябва да се прилагат само след адекватно инициално мониториране на виталните показатели и детайлна анамнеза за сърдечносъдови и дихателни проблеми. Проследяването трябва да продължи и по време на самото лечение.
Imiquimod 5% крем
Imiquimod (имиквимод) е локален имуномодулатор, който активира имунната система на мястото на приложение чрез взаимодействие с toll-like receptor (TLR) 7 на дендритните клетки и продукцията на проинфламаторни цитокини и на антиангиогенния фактор тъканен инхибитор на матриксните металопротеинази (19). Imiquimod има и антипролиферативен и антиангиогенен ефект (20).
Imiquimod 5% може да се прилага за лечение на детски хемангиоми по схема, като се започва с 3 пъти седмично за 4 седмици с увеличаване честотата на приложение след началния период. Честотата и продължителността на лечението трябва да се индивидуализират в зависимост от клиничното повлияване и степента на иритация. При изразена иритация лечението временно се преустановява до овладяване на локалните симптоми, за да се намали рискът от цикатризиране.
Imiquimod 5% крем има добър профил на безопасност при децата. Страничните ефекти са подобни на тези при възрастните и се изразяват главно в иритация на мястото на приложение с локален еритем, крусти и контактен дерматит (21). Фармакокинетичните проучвания при бебета и деца показват, че системната резорбция след локално приложение е много ниска и в повечето случаи не води до засягане и поява на симптоми от страна на вътрешните органи (21, 22). Най-често наблюдаваните системни странични ефекти са преходни грипоподобни симптоми и по-специално повишаване на температурата (23).
Лечение на улцерации
Улцериране е най-често наблюдаваното усложнение на хемангиомите в кърмаческа възраст и засяга до 15,8 % от децата (24), като в 83.1% от случаите се развива през пролиферативната фаза (25). Рискови фактори за улцериране са големи размери, смесен или сегментен тип, локализация на долната устна, врата или в аногениталната област. Провеждането на лечение е необходимо, тъй като тъканната деструкция води до повишен риск от локална или системна инфекция, кървене, болка и цикатризиране (24, 25).
Конвенционалният подход при улцериране на хемангиома включва грижа за нарушената повърхност с локални антисептици и превръзки, приложение на локални кортикостероиди или лазерно лечение (26). При големи хемангиоми улцерацията може да се повлияе от интерферон и винкристин (26).
Propranol, приложен перорално в стандартната доза на лечение, също е показал значителна ефективност за реепителизация при улцерации с пълно заздравяване за 2 до 4 седмици (27). Системното лечение се провежда в комбинация с локални антисептици и превръзки.
Заключение
Хемангиомите при деца и кърмачета обикновено протичат доброкачествено, но често представляват терапевтичен проблем, когато налагат лечение. Пероралните кортикостероиди дълги години са били средство на избор при лечението на хемангиомите. Случайното откриване на значителната ефикасност и сравнително добра безопасност на пропранолол при тези пациенти обаче променя напълно терапевтичния подход. Въпреки краткосрочния опит и малкия брой пациенти повечето автори предпочитат пропранолол пред системните кортикостероиди поради сравнително по-благоприятния и щадящ профил на безопасност. Изборът на лечение за всеки пациент трябва да се индивидуализира според типа, състоянието и разположението на хемангиома, както и според индивидуалните особености на детето.
Въвеждането на нови терапевтични средства и оптимизирането на терапията при деца с хемангиоми ще доведе до по-успешна профилактика на козметичните и животозастрашаващи усложнения. Въпреки това липсата на достатъчно данни от клиничната практика и от стандартизирани клинични изпитвания налага внимателна оценка на отношението полза/риск от прилагането на различните средства за терапия или активната ненамеса.
Библиография
1. Storch CH, Hoeger PH. Propranolol for infantile haemangiomas: insights into the molecular mechanisms of action. Br J Dermatol. 2010; 163: 269-274.
2. Kilcline C, Frieden I. Infantile hemangiomas: how common are they? Ped Dermatol. 2008; 25: 168-173.
3. Drolet BA, Swanson EA, Frieden IJ, et al. Infantile haemangiomas: an emerging health issue linked to an increased rate of low birth weight infants. J Pediatr. 2008; 153: 712-15.
4. Zimmermann AP, Wiegand S, Werner JA, Eivazi B. Propranolol therapy for infantile haemangiomas: Review of the literature. J Ped Otorhinolaryngol. 2010; 74: 338-342.
5. Schwartz RA, Sidor MI, Musumeci ML, et al. Infantile haemangiomas: a challenge in paediatric dermatology. J Eur Acad Dermatol Venereol 631-8. 2010; 24: 631-8.
6. Maguiness SM, Frieden IJ. Current management of infantile hemangiomas. Semin Cutan Med Surg. 2010; 29: 106-114.
7. Boye E, Jinnin M, Olsen BR. Infantile hemangioma: Challenges, new insights, and therapeutic promise. J Craniofac surgery. 2009; 20: 678-684.
8. Léauté-Labrèze C, Dumas de la Roque E, Hubiche T, et al. Propranolol for severe hemangiomas of infancy. N Engl J Med. 2008; 358: 2649-51.
9. O’Loughlin A, O’Donnell B, Watson R. Mature infantile haemangiomas role for propranolol. J Eur Acad Dermatol Venereol. 2010; 25: 1363-4
10. Storch CH, Hoeger PH. Propranolol for infantile haemangiomas: insights into the molecular mechanisms of action. Br J Dermatol. 2010; 163: 269-74.
11. Love JN, Sikka N. Are 1-2 tablets dangerous? Beta-blocker exposure in toddlers. J Emerg Med. 2004; 26: 309-14.
12. Lawley LP, Siegfried E, Todd JL. Propranolol treatment for hemangioma of infancy: risks and recommendations. Pediatr Dermatol. 2009; 26: 610-4.
13. Holland KE, Frieden IJ, Frommelt PC, et al. Hypoglycemia in children taking propranolol for the treatment of infantile hemangioma. Arch Dermatol. 2010; 146: 775-8.
14. Bonifazi E, Acquafredda A, Milano A, et al. Severe hypoglycemia during successful treatment of diffuse hemangiomatosis with propranolol. Pediatr Dermatol. 2010; 27: 195-6.
15. Sans V, de la Roque ED, Berge J, et al. Propranolol for severe infantile hemangiomas: follow-up report. Pediatrics. 2009; 124: e423-31.
16. Holmes WJ, Mishra A, Gorst C, Liew SH. Propranolol as first-line treatment for rapidly proliferating infantile haemangiomas. J Plast Reconstr Aesthet Surg. 2011; 64: 445-51
17. Schiestl C, Neuhaus K, Zoller S, et al. Efficacy and safety of propranolol as first-line treatment for infantile hemangiomas. Eur J Pediatr. 2011; 17: 493-501.
18. Zimmerman TJ, Kooner KS, Morgan KS. Safety and efficacy of timolol in pediatric glaucoma. Surv Ophthalmol. 1983; 28: 262-264.
19. Hurwitz DJ, Pincus L, Kupper TS. Imiquimod: a topically applied link between innate and acquired immunity. Arch Dermatol. 2003; 139: 1347-50.
20. Sidbury R, Neuschler N, Neuschler E et al. Topically applied imiquimod inhibits vascular tumor growth in vivo. J Invest Dermatol. 2003; 121: 1205–1209.
21. McCuaig CC, Dubois J, Powell J, et al. A Phase II, Open-Label Study of the Efficacy and Safety of Imiquimod in the Treatment of Superficial and Mixed Infantile Hemangioma. 2009; 26: 203-212.
22. Myhre PE, Levy ML, Eichenfield LF et al. Pharmacokinetics and safety of imiquimod 5% cream in the treatment of molluscum contagiosum in children. Pediatr Dermatol. 2008; 25: 88–95.
23. Barry RBM, Hughes BR, Cook LJ. Involution of infantile haemangiomas after imiquimod 5% cream. Clin Exp Dermatol. 2008; 33: 446–9.
24. Chamlin SL, Haggstrom AN, Drolet BA, et al. Multicenter prospective study of ulcerated hemangiomas. J Pediatr. 2007; 151: 684-9.
25. Hermans DJ, Boezeman JB, Van de Kerkhof PC, et al. Differences between ulcerated and non-ulcerated hemangiomas, a retrospective study of 465 cases. Eur J Dermatol. 2009; 19: 152-6.
26. Thomas RF, Hornung RL, Manning SC, Perkins JA. Hemangiomas of infancy: treatment of ulceration in the head and neck. Arch Facial Plast Surg. 2005 r., Том 7, стр. 312-5.
27. Naouri M, Schill T, Maruani A, et al. Successful treatment of ulcerated haemangioma with propranolol. J Eur Acad Dermatol Venereol. 2010 r., Том 24, стр. 1109-12.






