Брой 4/2016
Проф. д-р Златко Кълвачев, дмн
Причините, водещи до малигнена клетъчна трансформация са разнообразни – от спонтанна промяна при случайни мутации и пренареждане на гени, до насочена индукция от различни химични, физични или биологични агенти, наричани канцерогени. Изучаването им продължава през годините, като особено място заема интересът към инфекциозните причинители на рака – вируси и бактерии. За възможна инфекциозна етиология на рака се съобщава още в края на 19-ти век, когато се представят „доказателства”, че някои от известните по онова време причинители на заразни болести превръщат нормалната клетка в ракова. Дори Scheuerlen (1886 г.) описва “бактерии на рака”, които по-късно се оказват сапрофити.
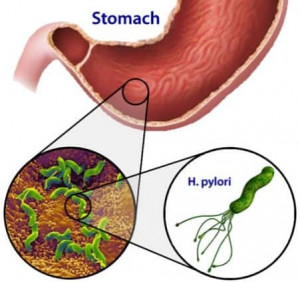
След откриването на Helicobacter pylori от австралийците Warren и Marshall, проучванията доказаха, че този бактерий унищожава не само лигавицата, но е и силен канцероген. Продължаващата хеликобактериална инфекция увеличава риска от развитие на стомашен рак от 2 до 3 пъти. Инфекцията е много разпространена – всеки 3-4 от 10 души в Европа (т.е. 30-40%) са инфектирани. Това е причината за огромния научен и обществен интерес към проблема – към днешна дата има около 2 млн. съобщения в Интернет по темата. Днес се знае, че H. pylori е тясно свързан с развитието на аденокарциномите и лимфомите на стомаха.
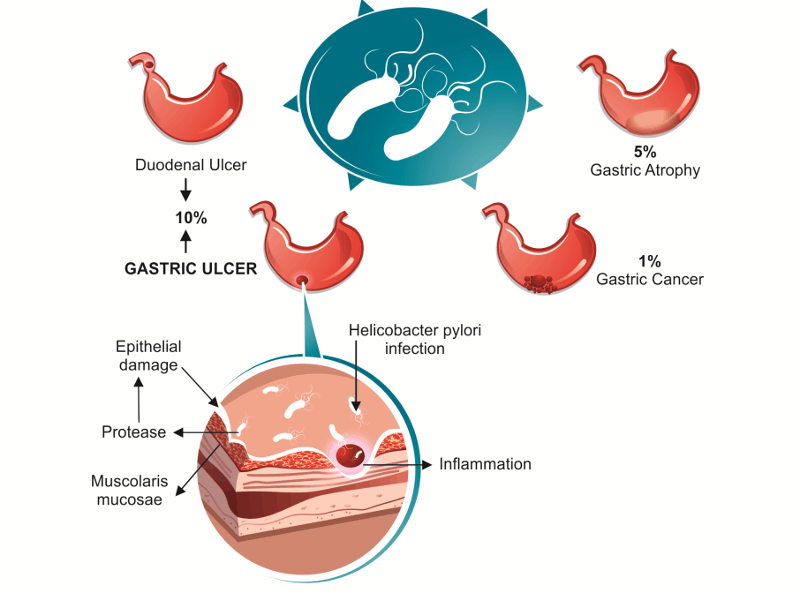
Инфекцията с H. pylori се свързва с индуцирането на стомашна карциногенеза, като това се дължи както на директното, така и на индиректното въздействие на микроорганизма върху епителните клетки на стомаха – възпаление на лигавицата и индукция на протеинова модулация и генни мутации.
H. pylori-асоциирания стомашен рак винаги се предшества от гастрит, като рискът за развитието на карцином е пропорционален на тежестта на гастрита. Освен с инфилтрация на Т-лимфоцити и активирани мононуклеарни клетки, индуцираният от H. pylori гастрит се характеризира още със засилено производство на различни проинфламаторни цитокини в стомашната лигавица, някои от които (като IL-бета1) се свързват с индуцирането на карциногенеза. Продукцията на други цитокини – тумор-некротизиращ фактор-алфа (TNF-алфа), IL-6, IL-7 и IL-8, също е повишена в стомашната лигавица, като IL-бета1 и TNF-алфа повишават активацията на NF-кB (нуклеарен фактор-kappa B), за която се знае, че участва във възпалително-асоциираната карциногенеза. NF-кB участва в развитието на рака на стомаха на фона на гастрит, посредством своето анти-апоптозно действие в епителните клетки. H. pylori въздейства и върху клетъчните мембрани, като някои от ефектите се медиират от повърхностните клетъчни рецептори, като Toll-like рецепторите (TLR).
Проучвания за вирулентността на H. pylori и патогенезата на язвената болест показват наличието на антитела, които са специфично насочени срещу два от протеините на H. pylori – cagA и vacA. Освен това, развитието на стомашен рак се характеризира с натрупване на генни модулации и мутации. Различни генни мутации, като например тези в TP53, се откриват при карцином на стомаха, като TP53 генната мутация присъства в почти 50% от случаите на стомашна неоплазия.
Установено е, че H. pylori директно индуцира генни мутации чрез засилване експресията на активирано-индуцираната цитидинова деаминаза в стомашните епителни клетки. Този фактор е от съществено значение за соматичните хипермутации и играе ролята на превключвател на имуноглобулиновите гени в В-лимфоцитите.
Взети заедно, тези данни категорично показват, че H. pylori директно индуцира генни мутации в епителните клетки. Проучванията доказват, че инфекцията с H. pylori повишава аберантната ДНК метилация в лигавицата на стомаха и че този процес може да участва в стомашната карциногенеза чрез намаляване на тумор супресорните гени.
В заключение трябва да се каже, че днес, 130 години след първите опити да се свържат инфекциите и рака, най-добрата стратегия за предотвратяване на рака на стомаха е ерадикацията на H. pylori. Препоръчително е това да става още в ранната фаза на инфекцията, тъй като за развитието на неоплазията важна роля играят генните промени, които могат да се индуцират в този период.